アルカンのスルホン化反応 彼らです 有機置換反応、生産を目的として実施 スルホン酸 (SO基を持つ有機化合物3炭素原子または炭素鎖に結合したH)および水(H2O)。
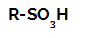
スルホン酸の構造式
スルホン化反応を行うため アルカン、アルカン(炭素原子と水素原子のみで飽和した炭素鎖によって形成される化合物)と 硫酸 (H2のみ4)濃縮され、加熱されます(Δ)。
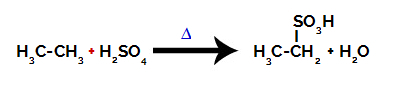
2炭素アルカンのスルホン化を表す化学式
アルカンのスルホン化反応の原理
といった アルカンスルホン化反応 それは置換反応であり、小さな成分間の交換があります 電気陰性度 反応物の、すなわち、アルカンと硫酸の間。 アルカンには水素と硫酸、スルホン酸基があります。
以下に、のメカニズムのステップバイステップがあります アルカンのスルホン化反応. 例として、最も単純なアルカンであるメタン(CH4):
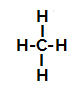
メタンの構造式
最初のステップ: 硫酸中のヒドロキシル(OH)と硫黄(S)の間の結合の破壊。
硫酸に存在する各ヒドロキシル基は、より電気陰性であるという特徴があります。 反応中の加熱により、ヒドロキシル基と硫黄の間の結合が切断される傾向があります。
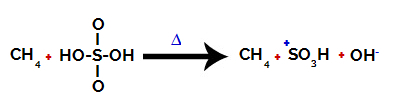
硫黄とヒドロキシルの間の結合の破壊
ただし、構造内の電子的再配列のため、すべてのヒドロキシルの結合の切断は発生しません。 次に、水酸化物アニオン(OH)が得られます。-)およびスルホン酸カチオン。
2番目のステップ: アルカン分子に対するヒドロキシル基の攻撃。
次にヒドロキシ基(OH-)アルカンを攻撃し、炭素と水素(電気陰性度の違いにより壊れやすい)の結合を切断します。
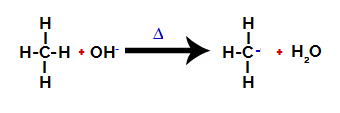
アルカンの炭素と水素の間の結合を壊す
注意: 炭素と水素の間の結合の破壊は、電子密度または電荷が低い炭素で常に最も頻繁に発生します。 炭素の水素が少ないほど、または炭素に結合している基が多いほど、その電子密度は低くなります。 だから私たちは持っています:
三次炭素
結合が切断された後、アルカンは電子不足の炭素になります(カルボカチオン)。 水酸化物基(OH)-)放出された水素と相互作用し、水分子を形成します。
3番目のステップ: 形成されたラジカルのスルホン酸基への攻撃。
最後に、スルホン酸基が残りのアルカンによって攻撃され、スルホン酸を形成します。
今やめないで... 広告の後にもっとあります;)
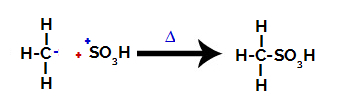
相互作用してスルホン酸を形成する構造
アルカンのスルホン化反応を表す方程式の例
最初の例: プロパンのスルホン化。
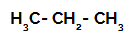
プロパンの構造式
プロパンには2つの一次炭素と1つの二次炭素があり、それらは異なる量の水素に結合しているため、電荷が異なります。 炭素は水素よりも電気陰性度が高いため、これらの炭素の電子密度は異なります。
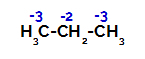
プロパンの各炭素原子の電荷の分布
一次炭素では、電荷は-3(3つの水素に結合しているため)であり、二次炭素では、電荷は-2(2つの水素に結合しているため)です。 したがって、炭素と水素の間の結合が切断され、場合によっては(1つの分子の)炭素1で、場合によっては(別の分子の)炭素2で切断されます。
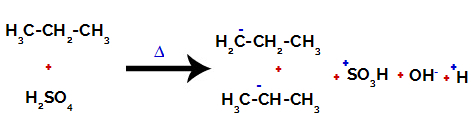
異なる炭素上の炭素と水素の間の結合を切断する
硫酸とアルカンの両方で結合が切断された後、 炭素1の水素がスルホン酸基で置換された製品。同じことが炭素でも起こります。 2.
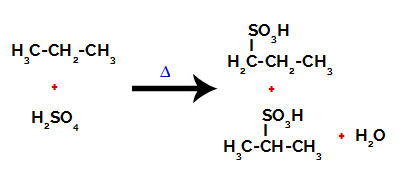
プロパンのスルホン化から形成された生成物
2番目の例: 2-メチル-ブタンのスルホン化。

2-メチルブタンの構造式
2-メチルブタンには、2次炭素と3次炭素の3つの一次炭素があります。 次の構造に見られるように、異なる電荷、したがって異なる電子密度。
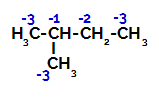
2-メチル-ブタンの電荷の分布
したがって、2-メチルブタンには、炭素と水素の間の結合を切断するいくつかの可能性があります。 これは、(分子の)炭素1、(別の分子の)炭素2、炭素3、または炭素で発生する可能性があります 4. ただし、炭素数2での破壊がより一般的であることは注目に値します。
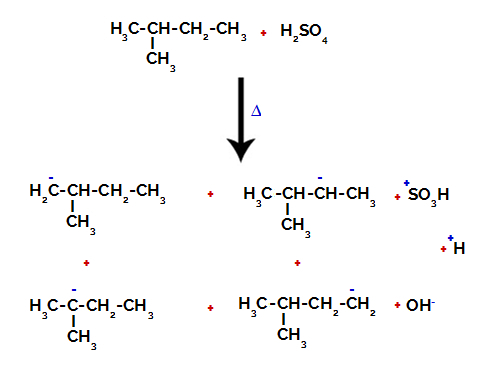
異なる炭素上の炭素と水素の間の結合を切断する
硫酸とアルカンの両方で結合が切断された後、 炭素1の水素がスルホン酸基で置換された製品。同じことが カーボン2。

2-メチル-ブタンのスルホン化から形成された生成物
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "アルカンのスルホン化反応"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/reacoes-sulfonacao-alcanos.htm. 2021年6月28日にアクセス。