物質(原子)の構成についての考えは、紀元前450年頃の古代ギリシャで現れました。 a。、主にデモクリトスとレウキッポスから。 しかし、原子は実際にはいわゆる科学的特徴を受け取った後にのみ ダルトンの原子理論.
THE ダルトンの原子理論 それは他の科学者が原子とその特性を知るための基礎として役立ったので、それは原子知識の発展の基礎でした。
誰だった ジョン・ドルトン?
訓練を受けた化学者のジョン・ダルトンは、1766年にイギリスのカンブリアで生まれ、1844年にマンチェスターで亡くなりました。 幼い頃から、彼の人生は科学的な研究と教育に運命づけられていたので、彼はさまざまな知識分野の開発に教えたり貢献したりしました。
しかし、科学者としての彼の最大の遺産は、最初の原子理論の開発でした。 ダルトンの原子理論が1808年に登場したのは、ガスの混合とラヴォワジエによって提案された研究の知識に関連するいくつかの実験を通してでした。
ダルトンの原子理論の仮定
ダルトンの原子理論は実験に基づいていましたが、これらの実験のどれも原子を明確に明らかにすることはできませんでした。 したがって、ダルトンは原子を物質の最小部分と呼んだ。
ダルトンの理論は、証明よりもはるかに多くの仮定を提示します。 それらのいくつかを参照してください:
原子は巨大で球形です(ビリヤードボールに似ています)。
原子は不可分です。
原子は破壊できません。
1 化学元素 これは、同じプロパティ(サイズと質量)を持つ原子のセットです。
異なる化学元素の原子は、互いに異なる特性を持っています。
2つの原子の相対的な重みを使用して、それらを区別できます。
化合物化学物質は、異なる種類の原子の同じ組み合わせによって形成されます。
異なる原子を組み合わせることにより、異なる化学物質が形成されます。
ダルトン原子モデルの表現
ダルトンは彼の原子モデルをビリヤードボールと名付けたので、球形の記号によって彼の時代に知られている元素の原子を表現し始めました。
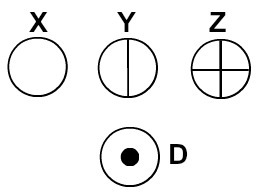
ダルトンの原子理論に従って表された原子
特定の詳細を持つ各原子表現は、異なる化学元素を示します。 初級および中級レベルの本と演習では、原子を異なる色の球でのみ表現しています。
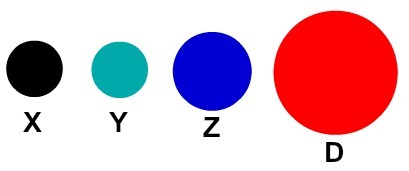
原子の教訓的表現
ダルトンの原子理論の貢献
の理解 ラヴォワジエの質量保存の法則
フランスの化学者ラヴォワジエは1785年に次のように主張しました 「化学反応では、原子の生成も破壊もないため、質量が節約されます。 ”. ダルトンの原子理論は、彼の仮定の1つが原子は破壊できないと述べているので、この事実を証明しました。
したがって、酸素ガス(O)の存在下で石炭(C)の燃焼を行うと2)、1つの炭素原子と2つの酸素原子の間で化学反応が起こります。 この反応は二酸化炭素(CO2)、これは反応前の物質を構成していたのとまったく同じ原子を持っています。
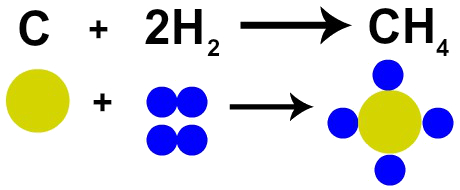
ダルトンの原子モデルによるラヴォワジエの法則の表現
の理解 単純な物質
を使用して ダルトンの原子モデル、 単体、つまり同じ特性の原子が分子を形成している物質を理解することができます。 したがって、同じ化学元素に属する原子があります。
物質Fで2たとえば、フッ素原子が2つあるため、ダルトンの原子理論による表現では、2種類の等しい原子を使用する必要があります。

による単体表現 ダルトンの原子モデル
の理解 複合物質
複合物質には、分子を形成するさまざまな特性の原子があります。 したがって、物質を形成するさまざまな化学元素があります。
物質H2たとえば、Oには3つの原子があります。2つは水素、もう1つは酸素です。 ダルトンの原子モデルによるその表現を参照してください。
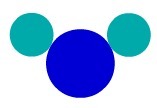
肌に合わせた複合物質の表現ダルトンの原子モデル
混合物を理解する
ダルトンの原子理論による混合物(2つ以上の異なる物質の結合)の理解は簡単です。2つの異なる分子を同じ容器に入れるだけです。

2番目の混合物の表現 ダルトンの原子モデル
ジョン・ドルトンによるその他の科学的貢献
の概念を導入しました 原子質量;
ガスの分圧の法則を定式化(ドルトンの法則);
と呼ばれる視覚障害を発見 色覚異常;
さまざまな温度での蒸気とガスの挙動を研究しました。
彼は、すべてのガスが同じように空間内で膨張する(特定の場所を占有しようとする)ことを発見しました。
私によって。DiogoLopesDias
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/teoria-atomica-dalton.htm
