THE 加水分解定数 (Kh)は 化学バランス 塩の加水分解(可溶性の塩と水が関与する化学反応)から確立されます。
他の平衡の定数として、 加水分解定数 次のように、生成物濃度の積を試薬濃度の積で割ったものから構成されます。
Kh = 【商品】【商品】
【試薬】
加水分解定数の操作には、次の3つの重要な現象に関する知識が必要です。
- 塩の解離;
- 水のイオン化;
- 塩の加水分解。
塩の解離
可溶性塩を水に加えると、ヒドロニウム(H +)以外の陽イオンとヒドロキシル(OH-)以外の陰イオンが解離して放出されます。

塩が水に溶けるか溶けないかを思い出させるために、 ここをクリック 塩溶解度表を調べます。
水のイオン化
水は自然に自己イオン化現象を起こす物質で、ヒドロニウムカチオンとヒドロキシルアニオンを生成します。
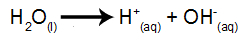
水イオン化式
塩の加水分解
可溶性塩として、それはイオンを水中に放出し、水はイオン化を受けて、生成します イオン 途中で、塩イオンと水イオンの反応(加水分解)が起こります。 この反応が発生した場合、考えられる相互作用は次のとおりです。
- 水の陰イオンによる塩の陽イオン(塩基の形成);
- 水の陽イオンと塩の陰イオン(塩の形成);
上記の相互作用は、形成された塩基または酸が弱い場合にのみ発生します。
塩の加水分解の例を参照してください。
→次亜塩素酸アンモニウム(NH4ClO)の加水分解
次亜塩素酸アンモニウムを水に加えると、溶解して解離し、アンモニウムカチオンイオン(NH4 +)と次亜塩素酸アニオン(ClO-)を放出します。

次亜塩素酸アンモニウムの解離で放出されるイオンを示す式
水はイオン化を受けるとH +とOH-を生成するため、溶液中に2つの陽イオンと2つの陰イオンがあり、これらは反応する可能性があります。 NH4 +カチオンは、弱塩基(NH4OH)を形成するため、OH-アニオンとのみ反応します。 ClO-アニオンは、弱酸(HClO)を形成するため、H +カチオンとのみ反応します。

次亜塩素酸アンモニウムの加水分解平衡式
加水分解定数の発現の構築
塩の加水分解定数の構築は、その塩の加水分解方程式にのみ依存します。 たとえば、前の項目で取り組んだ次亜塩素酸アンモニウムの加水分解により、次の式が生成されました。

次亜塩素酸アンモニウムの加水分解平衡式
の表現を構築する方法 加水分解定数 製品と試薬を考慮に入れると、定数の式は次のようになります。
Kh = [HClO]。[NH4OH]
[ClO-]。[NH4 +]
注:水は液体試薬であり、加水分解の発生の基本的な手段であるため、つまり一定であるため、方程式には含まれません。
私によって。DiogoLopesDias
ソース: ブラジルの学校- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-constante-hidrolise.htm