THE 角度ジオメトリ のいくつかのタイプの1つです 分子構造、線形、ピラミッド型、フラット三角型、 四面体、など。 角度ジオメトリは、次の特性を持つ分子にのみ見られます。
三原子分子、つまり、原子は3つしかありません。
中心原子に少なくとも3つの電子雲があります。
注意: 電子クラウドがすべてです 共有結合 (単一、二重、三重または座標)の原子と電子対の間 原子価層 通話に参加していない人。
角度のあるジオメトリを持つ分子の例をいくつか参照してください。
最初の例: 水(H2O)

従来の水構造
水の構造には、次のものがあります。
3つの原子:2つの水素と1つの酸素。
酸素は、結合の数が多いため(VIAファミリーに属するため2つ)、中心原子です。
酸素と水素の間の2つの単結合。 これは、各水素が1つの結合しか作成できず、酸素が2つの結合を作成できるためです。
価電子に6つの電子があり、結合に2つしか使用しないため、酸素に4つの非結合性電子があります。
したがって、水分子の場合と同様に、中央の原子には3つの原子と4つの電子雲(2つの単結合と2つの非結合性電子のペア)があります。 ジオメトリは角度があります.
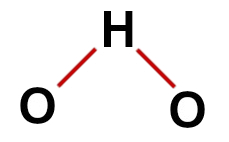
水の正しい構造式
注意: 分子がこれらのパターンを示すときはいつでも、原子間に形成される角度は約109º28です。'.
今やめないで... 広告の後にもっとあります;)
2番目の例: 二酸化硫黄(SO2)

二酸化硫黄の従来の構造
二酸化硫黄の構造には、次のものがあります。
3つの原子:2つの酸素と1つの硫黄原子。
硫黄は、すべての元素が同じ数(2つ)の結合を形成する必要があるため、分子内で最小の元素であるため、中心原子です。
硫黄と酸素の1つとの間の二重結合。 これは、両方に2つの接続が必要なためです。
1 配位結合または結合共有結合硫黄は他の酸素とペアリングした後は安定していましたが、2つの電子を必要とする酸素原子がまだ存在しているためです。
酸素中の4つの非結合電子。 これは、酸素が価電子シェルに6つの電子を持ち、結合に2つしか使用しないためです。
したがって、二酸化硫黄分子の場合と同様に、中央の原子には3つの原子と4つの電子雲(2つの単結合と2つの非結合性電子のペア)があります。 ジオメトリは角度があります.
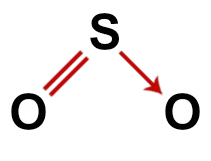
二酸化硫黄の正しい構造式
注意: 分子がこれらのパターンを持っているときはいつでも、原子間に形成される角度は約120です。O.
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "角度ジオメトリとは何ですか?"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-geometria-angular.htm. 2021年6月27日にアクセス。


