ガス理想的 は 衝突 粒子間は完全に弾力性があります. 彼の粒子の間には、次のような相互作用はありません。 力 さらに、魅力的または反発的であり、これらの粒子はスペースを占有しません。
による 気体の運動論、理想気体の熱力学的状態は、次の変数によって完全に記述されます。 圧力、ボリュームと 温度.
見てまた: 熱量測定:マインドマップ、数式、解決済みの演習
理想気体の概念
理想気体は専ら 粒子に寸法時間厳守 (ごくわずかなサイズの) 移動混沌としました オンになっています 高い速度。 このタイプのガスでは、粒子の温度と並進速度は比例します。
理想気体の粒子間に相互作用がないため、 内部エネルギー このガスのは常にの合計に等しい 運動エネルギー それを構成するすべての粒子の。
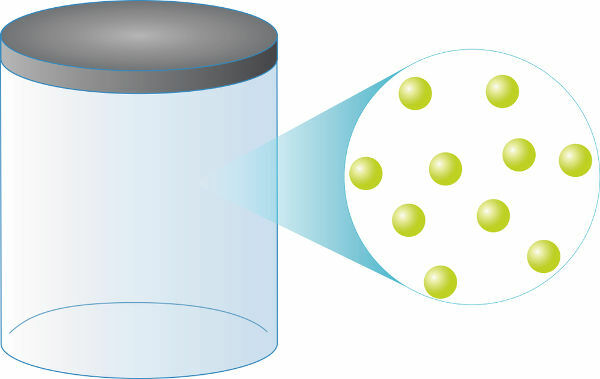
理想気体が何であれ、それらは常に同じです 数に粒子 同じボリュームに対して。 それらの質量は、順番に、あなたに直接依存します モル質量 (g / molで測定)さらに、 1モルの理想気体 (約6.0.1023 粒子)は常に 22.4リットルに等しい容量。
君は ガスリアル、 の発生がある場所 衝突非弾性 粒子間で、理想気体の振る舞いに非常に近づきます 低圧および高温領域。 偶然にも、地球の圧力と温度の通常の条件下(25°Cと1気圧)では、ほとんどの 気体は理想気体のように振る舞い、これにより熱力学的挙動に関する予測の計算が容易になります 彼らの。
のようないくつかのガス 水蒸気、 で希釈されています 大気ガス、理想気体とは見なされませんが、はい ガスリアル。 これらのガスは、粒子間に重要な相互作用があり、 凝縮する、それらを引き起こす 液化、 ある場合 温度低下.
今やめないで... 広告の後にもっとあります;)
理想気体の特性
でそれをチェックしてください 概要、理想気体のいくつかの特性:
- それらでは、粒子間の完全な弾性衝突のみが発生します。
- それらでは、粒子間の相互作用はありません。
- それらの中で、粒子の寸法はごくわずかです。
- 理想気体1モルは、気体が何であるかに関係なく、22.4リットルの体積を占めます。
- 実在気体は、低圧および高温状態では理想気体のように動作します。
- ほとんどのガスは理想気体と同様に動作します。
理想気体の法則
学者によって開発されたガスの研究 チャールズ
ボイル、ジョセフルイゲイルサック そして ロバートボイル の出現につながった 3つの経験則、の体制における理想気体の挙動を説明するために使用されます 温度, 圧力 そして ボリューム定数、 それぞれ。一緒にこれらの法律はの出現のために必要な基礎を形成しました 理想気体の法則、関連する ガスの初期熱力学的状態、量Pによって定義されます1、T1 およびV1、あなたと 最終的な熱力学的状態 (P2、V2 およびT2)、いくつか苦しんだ後 ガス変換.
をチェックしてください 式 一般気体の法則の:
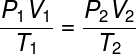
一般的な気体の法則は、 製品 与える 圧力 毛皮 ボリュームのガス、 ケルビン単位の熱力学的温度で割ると、定数に等しくなります。 この定数は、次のように記述されます。 クラペイロン方程式、 見る:
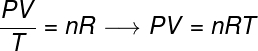
番号 –モル数(mol)
R –完全ガスの普遍定数(0.082 atm.l / mol。 Kまたは8.31J / mol。 K)
式では、 P ガスによって加えられる圧力です、 V このガスが占める体積であり、 T ケルビンで測定された温度です。 偉大さ 番号 モル数を指しますが、 R は理想気体の普遍的な定数であり、多くの場合、atm.l / molの単位で測定されます。 KまたはJ / mol。 K、後者はによって採用されています SI.
見てまた:太陽風とは何ですか?それは地球の大気にどのように影響しますか?
理想気体の内部エネルギー
THE エネルギー内部 理想気体の量は、次の間の積を使用して計算できます。 絶え間ないにボルツマン および熱力学的温度、注:
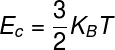
KB –ボルツマン定数(KB = 1,38.10-23 J / K)
以前の関係から、これにより、 平均運動エネルギー 理想気体の粒子から、次の式を導きます。これを使用して、 分子の平均二乗速度 与えられた温度Tに対する理想気体の注意:
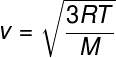
M –モル質量(g / mol)
この式により、次のことがわかります。 添加で温度 理想気体の その結果、粒子の平均二乗速度が増加します。
詳細:光が何でできているか、そしてその特徴は何であるかを調べてください
理想気体に関する解決済みの演習
質問1) 227°Cの温度で、1気圧の理想気体2モルが見つかります。 このガスが占める体積をリットルで計算します。
データ: R = 0.082 atm.l / mol。 K
a)75リットル
b)82 l
c)15リットル
d)27 l
e)25リットル
テンプレート: 文字B
解決:
このガスの体積を計算するには、クラペイロンの式を使用しますが、計算を行う前に、227°Cの温度をケルビンに変換する必要があります。 このために、この温度に係数273を追加すると、500Kの温度になります。
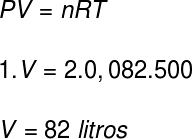
決議によると、ガスが占める体積は82リットルです。
質問2) 理想気体は、3 atmの圧力にさらされると、20 lの体積を占めるため、温度は一定に保たれ、体積は3倍になります。 この変換を経た後のこのガスの最終圧力を計算します。
a)1気圧
b)3気圧
c)5気圧
d)8気圧
e)9気圧
テンプレート: 文字a
解決:
この演習を解決するために、ガスの一般法則を使用します。注:
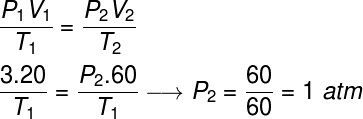
計算を行うには、変換中にガスの体積が3倍になるため、ガスに60リットルの体積を割り当てる必要がありました。
RafaelHellerbrock著
物理の先生