エントロピ これは、システムの無秩序の程度の尺度であり、エネルギーが利用できないことの尺度です。
に関連する物理量です 熱力学の第二法則 そしてそれは宇宙で自然に増加する傾向があること。
エントロピーの定義
「障害」は「混乱」としてではなく、システム組織の一形態として理解されるべきです。
エントロピーの概念は、常識に近いこの無秩序感を持つ他の知識分野に適用されることがあります。
たとえば、3つの瓶を想像してみましょう。1つは小さな青いビー玉、もう1つは同じ種類のビー玉で赤、3つ目は空です。
空のポットを取り、すべての青いボールを下に置き、すべての赤いボールを上に置きます。 この場合、ボールは色ごとに分けられて整理されています。
ポットを振ると、ボールが混ざり始め、ある瞬間に最初の分離がなくなりました。
ポットを振り続けても、ボールが同じ初期組織に戻る可能性は低いです。 つまり、順序付けられたシステム(色で区切られたボール)は無秩序なシステム(混合ボール)になりました。

したがって、自然な傾向は、システムの無秩序を増加させることであり、これはエントロピーの増加を意味します。 次に、システムでは次のように言うことができます。ΔS> 0、ここでSはエントロピーです。
また、それが何であるかを理解する エンタルピー.
エントロピーと熱力学
エントロピーの概念は、フランスのエンジニア兼研究者であるニコラ・サディ・カルノーによって開発され始めました。
機械的エネルギーの熱への変換、およびその逆の変換に関する彼の研究で、彼は完全に効率的な熱機械が存在することは不可能であることを発見しました。
THE 熱力学の第一法則 基本的に「エネルギーが節約される」と判断します。 これは、物理的なプロセスでエネルギーが失われることはなく、あるタイプから別のタイプに変換されることを意味します。
たとえば、機械はエネルギーを使用して仕事をし、その過程で機械は熱くなります。 つまり、機械的エネルギーは熱エネルギーに分解されています。
熱エネルギーは元に戻りません 力学的エネルギー (それが起こった場合、マシンは決してクラッシュしません)、したがって、プロセスは元に戻せません。
その後、ケルビン卿は熱力学的プロセスの不可逆性に関するカルノーの研究を補完し、 熱力学の第二法則.
ルドルフ・クラウジウスは、1865年にエントロピーという用語を最初に使用しました。 エントロピーは、 熱エネルギー それは特定の温度で機械的エネルギーに戻すことができない(仕事をすることができない)。
クラウジウスは、現在使用されているエントロピー()S)の変化の数式を開発しました。
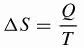
であること、
ΔS:エントロピー変動(J / K)
Q:伝熱(J)
T:温度(K)
あまりにも読む:
- 熱力学
- カルノーサイクル
- エネルギー
- エネルギーの種類
- 物理式
解決された演習
1)エネム-2016
1824年までは、蒸気エンジンや現在の燃焼エンジンなどの熱機関が理想的な動作をする可能性があると考えられていました。 Sadi Carnotは、100%の効率を得るために、2つの熱源(1つは高温でもう1つは低温)の間でサイクルで動作する熱機械の不可能性を実証しました。 このような制限は、これらのマシンが原因で発生します
a)機械的作業を実行します。
b)エントロピーが増加します。
c)断熱変換を使用します。
d)エネルギー保存の法則に違反する。
e)熱源と同じ温度で動作します。
代替案:b)エントロピーを増加させます。
2)エネム-2011
モーターは、別のシステムから一定量のエネルギーを受け取った場合にのみ機能します。 この場合、燃料に蓄えられたエネルギーの一部は燃焼中に放出されるため、アプライアンスは機能します。 エンジンが作動すると、燃焼で変換または変換されたエネルギーの一部を仕事に使用できなくなります。 これは、別の形でエネルギー漏れがあることを意味します。 カルヴァリョ、A。 バツ。 Z。
熱物理学。 ベロオリゾンテ:パックス、2009年(適応)。
テキストによると、エンジンの動作中に発生するエネルギー変換は、
a)エンジン内部の熱放出は不可能です。
b)エンジンによって実行される作業は制御できません。
c)熱を仕事に完全に変換することは不可能です。
d)熱エネルギーを動力学に変換することは不可能です。
e)燃料の位置エネルギー使用は制御できません。
代替案:c)熱を仕事に完全に変換することは不可能です。
も参照してください: 熱力学に関する演習


