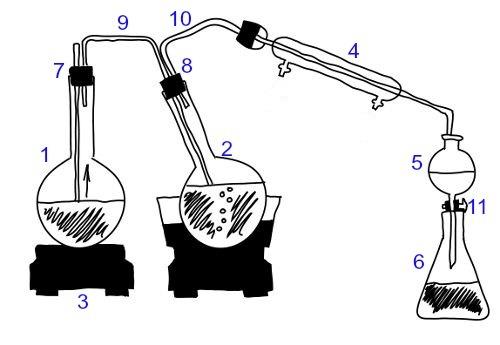
銅電極を囲む2つのバッテリーについて考えてみます。

亜鉛-銅および銅-銀電池。
ダニエル電池として知られる最初の電池では、電極は亜鉛と銅でできており、亜鉛が酸化される、つまり、銅に電子を供与するため、陽極になります。 次に、銅電極は陰極のように機能し、電子を受け取り、それ自体を還元します。
ただし、2番目のパイルである銅-銀電極では、銅がカソードとしてではなくアノードとして機能し、今回は酸化することが観察できます。
これは、これら3つの電極を比較すると、還元を受ける傾向が次のように機能することを示しています。
| 亜鉛 |
したがって、この還元を受ける能力は、 還元電位(E赤). この値は溶液の圧力、温度、濃度に依存するため、 標準電位 (または通常、25°C、圧力1atm、濃度1.0 mol / L)これは記号で識別されます そして0. 反対も当てはまります。 酸化電位(Eオキシ)、この場合は昇順です。
| 亜鉛>銅>銀 |
標準的な還元電位が低いほど、金属が電子を供与する能力が高くなり、その逆も同様です。 同様に、標準的な酸化電位が低いほど、金属が電子を受け取る能力が高くなり、逆もまた同様です。
| 山の中で、Eredが最も高い種は還元を受け、Eoxyが最も高い他の種は酸化を受けます。 |
上の図のような電圧計をこれらのセルの1つに適合させると、それらによって生成された電流の強度が測定されます。 起電力(emfまたはE)または電位差(Uまたはddp)*. 値はボルト(V)で示され、通常はバッテリーパックとラベルに表示されます。

ラベルに示されているバッテリーの電位差(Uまたはddp)。
起電力は、還元電位または酸化電位で表すことができます。 それを覚えておくことは重要です これらの電位は同じ値ですが、符号が逆です。
標準状態のバッテリーの電圧を計算するには、次の式を使用します。
| ∆そして0 = AND0赤(陰極) -そして0赤(アノード) |
または
| ∆そして0 = AND0オキシ(アノード) -そして0オキシ(カソード) |
したがって、各電極の絶対値は電圧計には表示されませんが、それらの間の電位差は表示されます。
*発電機の電位差の計算は次の式で与えられるため、起電力に等しい電位差を考慮します。U= E – r.i、ここで:
U =電位差
E =起電力
r =内部抵抗
i =電流強度
しかし、化学では、バッテリーを理想的な発電機と見なしているため、電気回路との関係でバッテリーの内部抵抗は無視できます。 したがって、U = Eとなります。
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/diferenca-potencial-uma-pilha.htm