等温変換では、 体積と圧力の変動 特定のガスの、しかし 一定温度; したがって、等温名の由来(ギリシャ語: iso =等しい; サーモ =熱)。
科学者のボイルとマリオットは、単独で同様の実験を行い、得られた結果は次のとおりでした。圧力が増加すると、ガスの体積が減少します。
たとえば、注射器のプランジャーについて考えてみてください。 このプランジャーに外圧を加えると、つまり圧力を上げると、シリンジ内に占める空気の量が減り、その逆も同様です。
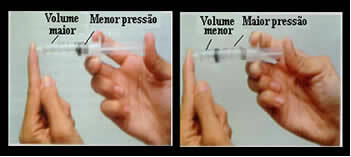
体積と圧力は反比例します。左側のパネルでは、圧力が小さく、空気が占める体積が大きくなっています。 右側では、シリンジプランジャーにさらに圧力を加えると、容量が減少します.
これは孤立したケースではなく、ガスに対して一般的な規則性で繰り返されるものです。 したがって、この事実は法律の形で述べられており、それは次のように説明することができます。
| ボイルの法則 または ボイル-マリオットの法則:一定の温度下では、ガスの固定質量が占める体積は、その圧力に反比例します。 |
これは、ガスの圧力を2倍にすると、その体積が半分になることを意味します。 そのような2つの量が反比例する場合、それらの積は定数です。 したがって、数学的には、この関係は次のように表すことができます。
| P.V = k |
ここで、k =定数です。
したがって、最初の状況で、特定のガスの圧力値がP1で、それぞれの体積がV1である場合、次のことを行う必要があります。
| P1. V1 = k |
この圧力をP2に上げると、その体積もV2に変更され、次のことを行う必要があります。
| P2 . V2 = k |
したがって、結論に達します。
| P1. V1 = P2. V2 |
この不変性は、次の表に示す、固定質量のガスの圧力と体積の例で確認できます。
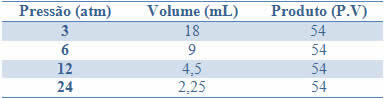
これらの値をグラフ化することにより、曲線の形成がわかります。
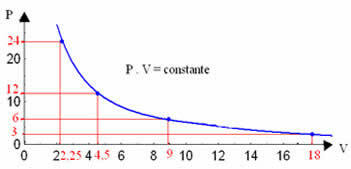
等温変換のグラフ表示は、実験が実行された圧力と体積および温度の値に関係なく、常に双曲線になります。 この双曲線はと呼ばれます 等温線; したがって、下のグラフに見られるように、温度が異なれば等温線も異なります。
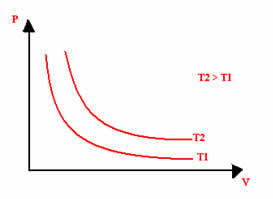
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/transformacao-isotermica-ou-lei-boyle.htm


