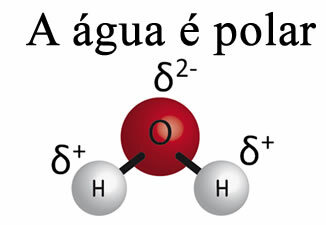
水だけでは材料からグリースを取り除くことはできません。 それの訳は ザ・水は極性です、下の画像に示すように、分子の水素原子と酸素原子の間に存在する電気陰性度の違いのため。 一方、 脂肪は無極性です したがって、水は脂肪を溶解しません。
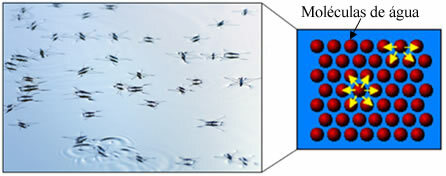
また、水には 表面張力. あなたはこれをテキストでよりよく理解することができます。 水の表面張力、しかし基本的には水面に形成される一種の弾性フィルムまたは膜であり、それが布や他の材料に浸透して汚れを取り除くのを防ぎます。 水分子は、を介してすべての方向に互いに引き付け合います 水素結合、しかし、表面分子は側面と下部の分子とのみ相互作用し、 凝集力、これにより、表面分子が収縮し、この表面張力が形成されます。
そこで石鹸と洗剤が登場します(ラテン語から) 解毒 =クリア)、これは 界面活性剤、それらは水の表面張力を低下させる能力を持っており、さらに、水と脂肪の両方と相互作用するためです。 これはどのように起こりますか?
石鹸と洗剤には脂肪酸塩が含まれています。脂肪酸塩は、 無極性部分 (とは 疎水性 – ハイドロ =水; 恐怖症= 嫌悪感)と 極性端 (親水性 – ハイドロ =水; 門= 友達)。 以下に、石鹸の典型的な構造を示します。
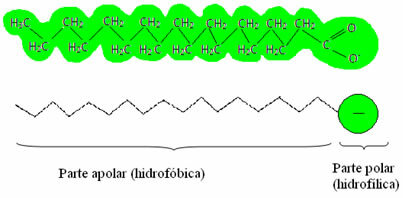
一般的に、洗剤は長鎖スルホン酸の塩です。
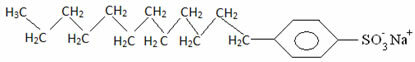
したがって、石鹸や洗剤に含まれるこれらの分子の非極性部分は、脂肪と相互作用します。 極性の端が水と相互作用し、それ自体を小さな小球にグループ化している間、 から呼び出された ミセル、親水性部分が水分子と接触しているミセルの外側に面している、および 脂肪は内側に留まり、非極性または疎水性の部分と接触します。これは、画像に示されているのと同様のプロセスです。 フォロー:
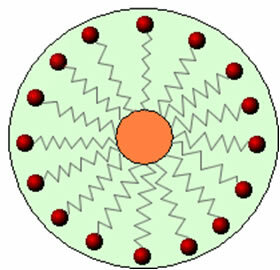
このようにして、脂っこい汚れがミセルの中心に閉じ込められ、取り除くことができます。 もう一つのポイントは、洗剤や石鹸には水の表面張力を下げる能力があるということです。 分子間の相互作用を減らし、さまざまな材料に浸透して分子を除去しやすくします。 泥。
ジェニファー・フォガサ
化学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/quimica-dos-saboes-detergentes.htm
