浸透圧検査 です 共有 (他は トノスコピー, ebullioscopy そして 凝固点降下)の発生を研究する 浸透 濃度の異なる2つの溶液の間で、一方が他方よりも濃縮されています。
注:束一性は、不揮発性溶質を溶媒に加えると発生します。
といった 浸透圧検査 浸透を研究するには、知ることが不可欠です とは この現象。 このために、半透膜で分離された以下のソリューションを使用します。
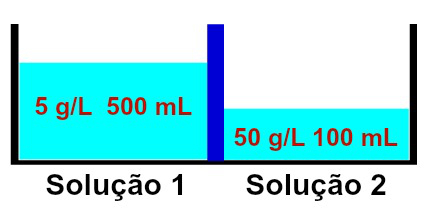
異なる濃度の溶液の表現
溶液1には5g / Lの濃度と500mLの容量が含まれているのに対し、 溶液2の濃度は50g / L、容量は100 mLで、メンブレンで分離されています。 半透性。 溶液2は溶液1よりも濃縮されているため、それらの間で浸透が発生する必要があります。
浸透は、溶液1の濃度が低いため、溶液1から溶液2に必ず発生する必要があります。 この発生中に、溶媒の一部が半透膜を通過し、溶液の体積が2になります。 両方の溶液が同じ濃度になり始めるまで、つまり、溶液1の量が増加し、減少します。 等張。

浸透の発生による溶液1および2の高さの変更
注:等張媒体は、濃度が等しい媒体です。
による 浸透圧検査、浸透は、低濃度の溶液中の溶媒の最大蒸気圧が高濃度の溶液中の溶媒の最大蒸気圧よりも高いために起こります。 ここで、浸透の発生を防ぎたい場合は、最も濃縮された溶液に圧力をかけるだけです。
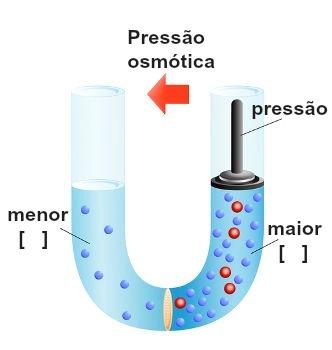
最も濃縮されたソリューションに対する圧力の実行の表現
浸透を遮断または逆浸透させるために最も濃縮された溶液に加えられるこの圧力は、 浸透圧 記号πで表されます。 溶液の濃度に正比例する必要があります。
浸透圧の可能な解釈
の結論によると 浸透圧検査、各溶液には浸透圧があります。これは、すべての溶液に存在する特性である濃度に関連しているためです。
ある媒体またはあるソリューションを別のソリューションと比較する場合、次の用語を使用できます。
高張:一方の媒体が他方よりも高い浸透圧を示す場合。
低張:一方の媒体の浸透圧が他方よりも低い場合。
等張:2つの媒体または溶液の浸透圧が同じ場合。
したがって、2つの溶液AとBの浸透圧を比較すると、 πTHE およびπB、私たちはそれを言うことができます:
AとBの浸透圧が等しい場合、平均または解は等張になります。
πTHE = πB
Aの浸透圧がBの浸透圧よりも大きい場合、媒体AはBに対して高張になります。
πTHE> πB
Bの浸透圧がAの浸透圧よりも低い場合、媒体BはBに対して低張になります。
πB< πTHE
浸透圧の計算式
π= M.R.T
この式では:
π=は浸透圧です
M =は mol / L単位の濃度
R =は一般的なガス定数です(気圧の圧力は0.082)。 圧力(mmHg)の場合は62.3)
T =ケルビン単位の温度
以下に示すように、mol / L単位の濃度には特定の式があります。
M = m1
M1.V
浸透圧の式で置き換えることができます。
π = m1.R.T
M1.V
注:溶液中に存在する溶質がイオン性である場合は、 ヴァントホフ補正係数 (i)浸透圧計算の表現において:
π= M.R.T.i
浸透圧計算の例
例: (UF-PA)25ºC、10mLの水に2mgの新しい抗生物質を含む溶液は、0.298mmHgの浸透圧を生成します。 したがって、この抗生物質の分子量は、おおよそ次のとおりです。
a)3000
b)5200
c)7500
d)12500
e)15300
演習で提供されたデータは次のとおりです。
π= 0.298 mmHg
T = 25 OCまたは298K(273で追加した後)
m1 = 2mgまたは0.002g(1000で割った後)
V = 10mLまたは0.01L(1000で割った後)
R = 62.3 mmHg
この演習を解決するには、次のように、浸透圧を計算するための式で使用可能なデータを適用するだけです。
π = m1.R.T
M1.V
0,298 = 0,002.62,3.298
M1.0,01
0.298.M1.0,01 = 37,1308
0.00298.M1 = 37,1308
M1 = 37,1308
0,00298
M1 = 12460 u
私によって。DiogoLopesDias
ソース: ブラジルの学校- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-osmoscopia.htm
