あ 昇華 これは、液相を通過せずに、固相から気相に直接移行することを特徴とする、物質の物理的状態の変化です。 厳密に言えば、どんな物質でも昇華できますが、特定の圧力と温度の条件下で起こります。 昇華は、固体によって発揮される分子間相互作用だけでなく、固相の蒸気圧とも相関します。
このプロセスは、固体の二酸化炭素で構成されるドライアイスで簡単に観察できます。 二酸化炭素は、加圧下および室温で昇華します。 昇華の反対のプロセスは、再昇華または堆積と呼ばれることがあります。 昇華が発生するには、物質がエネルギーを吸収する必要があるため、吸熱プロセスと見なされます。
こちらもお読みください: 物質の物理的状態は何ですか?
昇華についてのまとめ
昇華とは、液相を経由せずに、固相から気相に直接移行することです。
物質の昇華を観察するには、圧力と温度の特定の条件が必要です。
昇華は、固相の蒸気圧や分子間相互作用などの熱力学的側面の影響を受けます。
昇華は吸熱プロセスです。
昇華の一例は、固体の二酸化炭素からなるドライアイスで起こることです。
昇華とは?
昇華は 固相から気相への直接遷移、液相を通過せずに。 一部の固体では、特定の温度と圧力の条件下で発生します。 この遷移は、状態変化の物理的プロセスであり、化学反応を伴いません。
逆のプロセス、すなわち気相から固相への直接通過は、さまざまに呼ばれます。 この相変化に昇華という言葉を使う著者もいれば、「再昇華」や「沈着」を使用する著者もいます。
昇華のしくみ
昇華と蒸発の間に類似点を描くことができます。 どちらの場合も、エンドポイントは 気相. 明らかに、違いは開始段階にあります。昇華は固体、蒸発は液体です。
両方の場合において、 圧力の影響があります 熱と分子間相互作用を含む、蒸発と熱力学的側面。
蒸気圧とは?
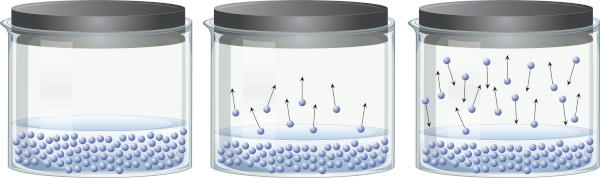
液体の入った密閉容器では、液相と気相の間に平衡があることがわかります。 これは、沸点以下であっても、存在するエネルギーが液体の一部の分子を分離して蒸気に移行するのに十分であるためです。 ただし、一部の蒸気分子は再び凝縮して液相に戻ることもあり、プロセスの可逆性を示しています。
この蒸気は、 物質(質量と体積がある)、演習 液体の表面の圧力、蒸気圧として知られています。 液体の量ではなく、温度に依存します。温度が高いほど、分子が液相から離れやすくなるためです。
常温で蒸気圧の高い液体を揮発性といいます。 たとえば、25°C では、エチル エーテルの蒸気圧は 0.58 atm、アセトン (プロパノン) の蒸気圧は 0.29 atm、水の蒸気圧は 0.023 atm です。 ちなみに、蒸気圧が大気圧と同じになると、液体は沸騰します。 蒸気圧の詳細については、クリックしてください。 ここ.
蒸気圧と昇華
程度は低いものの、 固体にも蒸気圧があります、しかし液体のそれよりはるかに低いです。 たとえば、1000 K の温度でも、鉄の蒸気圧はわずか 9.21 x 10 です。-20 気圧。 ただし、ヨウ素などの一部の固体はなんとか昇華し、常温でより高い蒸気圧を示します (4 x 10-4 気圧)。
これは、分子が固体状態から直接気体状態に移動する場合にのみ可能です。 これが起こるためには、 固体の分子が存在しなければならない 分子間相互作用 弱い (例えば、ヨウ素では、それらは誘導双極子誘導双極子タイプです)。
ことも見られる. 昇華プロセスは吸熱的です、つまり、固体の分子が熱の形でエネルギーを吸収して、分子間相互作用を壊して蒸気状態に移行できるようにする必要があります。 関連する熱量は、昇華エンタルピーとして知られる熱力学的量によって測定できます。
フェーズ図
に 固体の昇華が起こる圧力と温度の範囲を知ること、相図を評価する必要があります。 二酸化炭素、COの場合を見てみましょう2.

状態図では、状態 (固体、液体、および気体) 間の境界線が圧力と温度の値をまとめます。 状態変化が起こる. CO2 の場合を観察すると、1 気圧の圧力で固相が温度 -78.5 °C で気相に直接移行することがわかります。これは昇華の特徴です。
二酸化炭素は 5.11 気圧を超える圧力でのみ液相になり、その圧力を超えると昇華できなくなります。 相図の詳細については、 ここ.
昇華の例
ドライアイス: パーティーやイベントで霧の効果を作るためによく使用されるドライアイスは、実際には固体状態の二酸化炭素です。

防虫剤: 防虫剤は、芳香族有機化合物であるナフタレンから作られています。 悪臭を除去し、蛾、ゴキブリ、その他の有毒動物を追い払うために適用されるため、クローゼットや小便器でさえも使用されることが一般的です.

樟脳:特有の匂いがする樟脳小石も昇華することができます。 また、蚊を追い払い、カビを防ぐのにも役立ちます。

ヨウ素: ハロゲンに属する非金属も昇華します。

しかし、提示された物質の中で、 二酸化炭素のみが周囲条件下で昇華する. 他のものは、昇華があっても、私たちが住んでいる圧力の下で通常の融合を行うことができます.
こちらもお読みください: プラズマ — 物質の第 4 の状態
昇華に関する演習問題の解決
質問1
(Fuvest 2020) スーパーマーケットでは、果物、野菜、肉など、いわゆるフリーズドライ食品を見つけるのが一般的です。 フリーズドライ食品は、冷蔵しなくても長期間食べても大丈夫です。 これらの食品の「凍結乾燥」という用語は、凍結プロセスとそれに続く水の昇華による脱水を指します。 水の昇華が発生するには、線が相転移を表す圧力-温度グラフに示すように、条件の組み合わせが必要です。
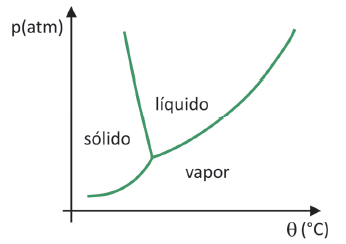
工業的に特定の技術の使用を必要とするプロセスであるにもかかわらず、人々が アンデス山脈の最も標高の高い地域に住んでいた先コロンブス人は、食べ物をフリーズドライにすることができました。 より多くの時間。 自然な凍結乾燥プロセスがどのように発生したかを説明する別の方法を確認してください。
a) 山岳地帯では気温が低く気圧が高いため、水の昇華が起こった。
b) 食物は寒い時期に自然冷凍された後、大気圧が低い山の最も低い場所に運ばれ、昇華が可能になりました。
c) 食品は太陽にさらされて温度が上昇し、局所的な大気圧が低いために凝固が促進されました。
d) 寒冷期には食物が凍るほど気温が低く、高山の気圧が低いため昇華が可能でした。
e) 食品を自然冷凍した後、プレスして圧力を上げ、昇華を起こさせた。
応答: 文字 D.
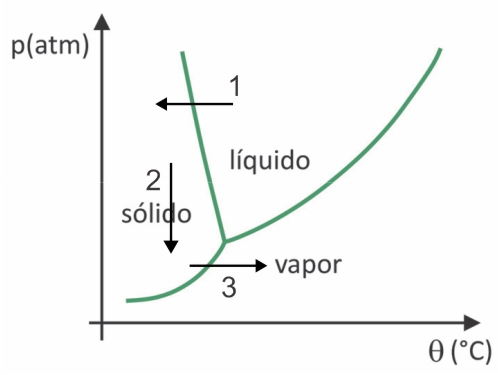
凍結乾燥では、水の凍結とその後の昇華があります。 コロンブス以前の人々は、冬に水が凍る可能性があるため、そのようなプロセスを実行できました(矢印1) そして、アンデスの最高地域の低圧 (矢印 2) により、昇華する可能性があります (矢印 3).
質問2
(Uerj 2005) 冷蔵プロセスで広く使用されているドライアイス、または凝固した二酸化炭素は、周囲条件下で昇華します。 この変換中に、エネルギーの変動や相互作用の破壊などの現象が発生します。
これらの現象は、それぞれ次のように分類されます。
a) 発熱 - イオン間
b) 発熱 - 核間
c) 等温 - 原子間
d) 吸熱 - 分子間
応答: 文字 D.
昇華は、固相分子をコンパクトに保つ相互作用を破壊するために熱を吸収する必要があるため、吸熱プロセスです。 これらの相互作用は分子間タイプのものです。
ステファノ・アラウホ・ノヴァイス
化学の先生

