純粋な物質は、単一の種類の化学種によって形成されます。つまり、その組成と特性は固定されています。 ミックスには複数のタイプのコンポーネントが含まれているため、その構成は異なります。
したがって、純粋な物質と混合物を区別できるのは、その組成がわかっている場合だけです。
コップ一杯の水とコップ一杯の溶かした砂糖を比較すると、私たちの目は違いに気づきません。 ただし、2つのグラスの内容物を摂取すると、一方が純粋な物質で、もう一方が混合物で構成されていることがわかります。
純粋な物質
純粋な物質とは、1つの化学種のセットです。つまり、他の化学種と混合されることはありません。
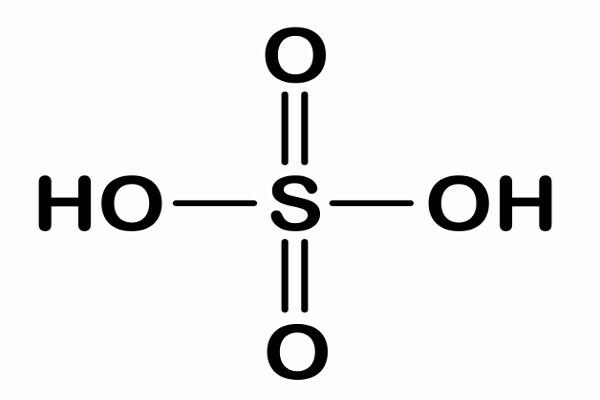
例として水を使用しましょう。 水(H2O)はその特性が認められており、この材料の特定の特性はそれを特定するのに役立ちます。 メイン 水の特性 彼らです:
| 密度 | 1.00 g / cm3 |
|---|---|
| 融点 | 0°C |
| 沸点 | 100°C |
材料が全体を通して固定された不変の特性を持っている場合、それは 純粋な物質.
食卓塩である塩化ナトリウム(NaCl)をコップ一杯の水に入れてかき混ぜると変化が起こります。

その結果、水と塩の密度の中間の密度の製品が得られます。 これは、水がもはや純粋な物質ではなく、 ミックス.
この混合物を凍結しようとすると、融解温度が0°C未満になり、 また、この混合物は100°Cで沸騰しません、これを蒸発させるためにより多くの熱が必要になります 製品。
純粋な単純および複合物質
純粋な物質は、その組成に化学元素が1つしかない原子がある場合、単純なものとして分類されます。
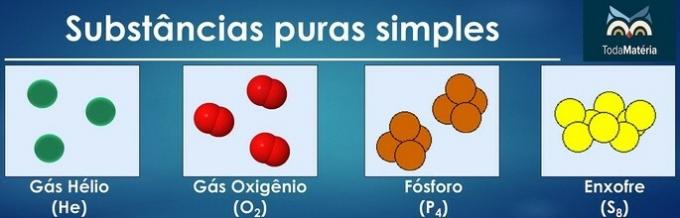
2つ以上の化学元素の原子の配置は純粋な複合物質を形成します。

混合物
混合物は、成分と呼ばれる2つ以上の純粋な物質の結合に対応します。
純物質とは異なり、混合物中の成分の比率に依存するため、その特性は固定されていません。
水と混合する塩の量によって、物理的特性である密度がどのように変化するかを確認してください。
| の塩の割合 混合物の総質量 |
混合密度(g / cm3) 20°Cで |
|---|---|
| 1 | 1,005 |
| 8 | 1,056 |
| 12 | 1,086 |
| 16 | 1,116 |
| 26 | 1,197 |
出典:FURNISS、B。 S。 etal。 フォーゲルの実用的な有機化学の教科書。 4. ed。 ロンドン:ロングマン、1987年。 P。 1.312.
したがって、水と塩の添加は、任意の比率で密度が変動するため、混合物を水または塩のいずれかに分類することはできません。
均一および不均一混合物
均一な混合物とは、成分を1つの相でのみ提示する混合物であり、したがって、すべての点で同じ特性を示します。

複数の相を視覚的に認識する場合、混合物は不均一として分類されます。

純粋な物質と混合物に関する要約
| 純粋な物質と混合物 | |
|---|---|
|
均一系 (1つのフェーズのみ) |
純粋な物質 (1つのコンポーネント) |
|
均一な混合物 (同じフェーズの複数のコンポーネント) | |
|
異種システム (複数のフェーズ) |
純粋な物質 (さまざまな物理状態のコンポーネント) |
|
不均一な混合物 (複数のフェーズで複数のコンポーネント) |
詳細については、これらのテキストを確認してください:
- 原子
- 化学元素
- 混合物の分離
コメント付きのフィードバックを含む演習
1. (UFMG)純粋な物質Xのサンプルでは、いくつかの特性が決定されました。 以下を除いて、すべての代替物には、この物質を特定するのに役立つ特性があります。
a)密度。
b)サンプルの質量。
c)水溶性。
d)沸騰温度。
e)融解温度。
間違った代替案:b)サンプルの質量。
a)正しい。 密度は、特定のボリューム内の物質の量です。 材料固有の特性として、物質の識別に役立ちます。
b)間違っています。 質量は、体内の物質量です。 この性質はいかなる物質にも適用されるため、その構成に関係なく、物質を特定するために使用することはできません。
c)正しい。 溶解度は、特定の液体に溶解する、または溶解しない物質の能力です。 材料固有の特性として、物質の識別に役立ちます。
d)正しい。 沸騰温度は、液体状態から気体状態への変化の温度に対応します。 材料固有の特性として、物質の識別に役立ちます。
e)正しい。 溶融温度は、液体から固体への変化温度に対応します。 材料固有の特性として、物質の識別に役立ちます。
2. (Vunesp)ミネラルウォーターのボトルのラベルを以下に再現します。
| 考えられる化学組成: |
|---|
| 硫酸カルシウム0.0038mg / L |
| 重炭酸カルシウム0.0167mg / L |
この情報に基づいて、ミネラルウォーターを次のように分類できます。
a)純粋な物質。
b)単体。
c)不均一な混合物。
d)均一な混合物。
e)コロイド懸濁液。
正しい代替案:d)均一な混合物。
a)間違っています。 その組成がH分子のみを含む場合、水は純粋になります2O。
b)間違っています。 単体は、1つの化学元素の原子で構成されています。 また、純水は水素原子と酸素原子(H)によって形成されるため、単体ではありません。2O)コンポジットとして分類されます。
c)間違っています。 不均一な混合物には複数の相があり、その場合、水しか観察できません。
d)正しい。 フェーズが1つしかないため、システムは均一です。 硫酸カルシウムと重炭酸カルシウムの化合物は水溶性であるため、水筒を見ると液体しか見えません。
e)間違っています。 コロイド懸濁液は、顕微鏡を使用して成分を区別する不均一な混合物です。
3. (UCDB)化学実験室では、次の混合物が準備されました。
私。 水/ガソリン
II。 水/塩
III。 水/砂
IV。 ガソリン/塩
V。 ガソリン/砂
これらの混合物のどれが均質ですか?
a)なし。
b)IIのみ。
c)IIおよびIII。
d)IおよびII。
e)IIおよびIV。
正しい代替案:b)IIのみ。
a)間違っています。 水は無機化合物であり、ガソリンは有機化合物です。 これらの物質は相互作用する能力がなく、密度が異なるため、不均一な混合物を形成します。
b)正しい。 塩である塩化ナトリウムは水に溶解し、均一な混合物である溶液を形成します。
c)間違っています。 砂、二酸化ケイ素は、水と不均一な混合物を形成します。
d)間違っています。 塩は無機化合物であり、ガソリンは有機化合物です。 これらの物質は相互作用する能力がなく、密度が異なるため、不均一な混合物を形成します。
e)間違っています。 砂は無機化合物であり、ガソリンは有機化合物です。 これらの物質は相互作用する能力がないため、不均一な混合物を形成します。
4. (Ufes)砂、塩、砂糖、水、ガソリンで構成されるよく混合されたシステムでは、相の数は次のとおりです。
a)2。
b)3。
c)4。
d)5。
e)6。
正しい代替案:b)3。
フェーズ1:塩と砂糖は水と相互作用することができ、分子間力によって分子が結合し、均一な混合物である溶液を形成します。
フェーズ2:水は無機化合物であり、ガソリンは有機化合物です。 これらの物質は相互作用する能力がなく、密度が異なるため、不均一な混合物を形成します。
フェーズ3:砂は、水やガソリンと化学親和力がないケイ酸塩であるため、フェーズを表します。
5. (マッケンジー)によって形成された混合物:
a)角氷と砂糖水溶液(ブドウ糖)。
b)Nガス2 およびCO2.
c)水とアセトン。
d)水とグーズベリーシロップ。
e)灯油およびディーゼル油。
正しい代替案:a)角氷と砂糖水溶液(ブドウ糖)。
a)正しい。 角氷とブドウ糖溶液の2つの相を観察することが可能であるため、それらは不均一なシステムです。
b)間違っています。 ガスは常に均一な混合物です。
c)間違っています。 プロパノンのカルボニルと水分子の間に水素結合が形成されます。 それらは極性物質であるため、アセトンは水に可溶化して均一な混合物を形成することができます。
d)間違っています。 水を加えることによって希釈が行われるため、グーズベリーシロップからの赤い液体のみが表示されるため、これら2つの成分が混合して均一なシステムを形成します。
e)間違っています。 どちらも有機化合物であり、化学親和力により単一相を形成し、均一なシステムを表します。
演習で知識をテストします。
- 均一および不均一混合物に関する演習
- 混合物の分離に関する演習
- 物質の性質に関する演習