sp型炭素の混成2 二重結合と2つの単結合、またはパイ結合(π)と3つのシグマ結合(σ)がある場合に発生します。 実際、spハイブリダイゼーション2 それは二重結合を確立する原子の間にもたらされます。
このような分子の例は、ホルムアルデヒド(CH2O)。 以下の構造に注意してください。
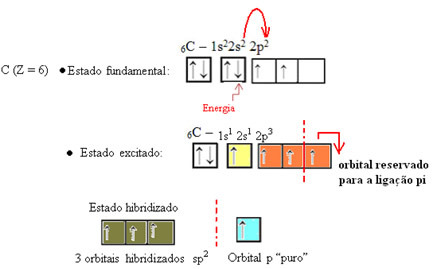
本文に見られるように「sp型ハイブリダイゼーション3」、炭素混成は、サブレベル2sからの電子がエネルギーを受け取り、 2pサブレベル、したがって、原子軌道の「混合」から4つの混成軌道を生成します ピュア。
ホルムアルデヒドの場合、パイ結合が存在することがわかっているため、これらの混成軌道の1つはこの結合用に予約され、他の3つはシグマ結合を持っています。
炭素と単結合を作る水素原子は、それらの軌道でそれを作ります:
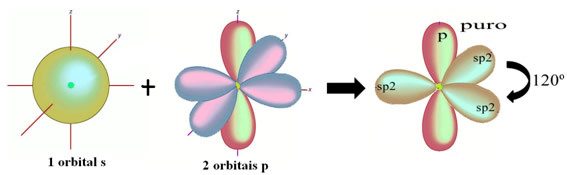
残りの「純粋な」p軌道は酸素原子を二重結合し、ホルムアルデヒド分子は次の構造を持っています。
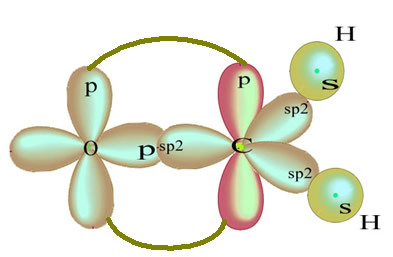
このホルムアルデヒド構造に存在する結合の種類については、次のとおりです。

接続: 1 = 2 = σs-sp2
3 = σp-sp2
4 =πp-p
ジェニファー・フォガサ
化学を卒業
ソース: ブラジルの学校- https://brasilescola.uol.com.br/quimica/hibridizacao-tipo-sp2.htm
