熱力学の第3法則は、エントロピーがゼロに近づく物質の挙動を扱います。
この法則によれば、システムが熱力学的平衡にあるときはいつでも、そのエントロピーはゼロに近づきます。
熱力学の第二法則はエントロピーに関連しています。 その後、3番目の法則は次のように表示されます エントロピーを決定する絶対基準点を確立しようとします.
Walther Nernst(1864-1941)は、熱力学の第3法則の基礎を形成する原理を扱った物理学者でした。
ネルンストによれば、純粋な物質の温度が絶対零度に等しいかそれに近い場合、エントロピーは最小値になる傾向があります。
そのために、ネルンストは以下の式を提案しました。これは、エントロピー(ΔS)と温度(T)の変動が最小値、つまり0になる傾向があることを示しています。
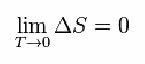
しかし、エントロピーとは何ですか?
エントロピ これは、分子がシステム内で組織化する方法です。 この組織は、混乱という意味ではなく、分子の動きと動揺という意味で無秩序に変換されます。
より多くの分子が移動できるほど、それらはより無秩序になり、より多くのエントロピーを持ちます。
当初、ネルンストは、彼が提案したエントロピーは完全結晶でのみ可能であると提案しました。
最後に、彼は絶対零度に等しい温度は存在しないと結論付けました。これは、第3の法則を物議を醸す法則にします。
したがって、多くの物理学者にとって、これは法律ではなく規則です。
非常に長い年月(1912年以降)の後、科学者はこの温度または絶対零度にますます近づく温度を取得しようとしています。 したがって、彼らはそれが気体でのみ可能であり、固体または液体状態の物質を廃棄することを発見しました。
あまりにも読んでください:
- 熱力学のゼロ法則
- 熱力学の第一法則
- 熱力学の第二法則
- 熱力学に関する演習