O 原子線 元素の数は、周期表の元素の位置に応じて変化する原子の半径を決定する周期的なプロパティです。
したがって、それらは増加および減少する可能性があります 原子番号 (Z)原子核に存在する陽子の数に対応する元素の。
要約すると、原子半径は2つの隣接する原子の原子核間の距離の半分に対応し、次のように表されます。
r = d / 2
whence:
r =半径
d =核間距離
一般に、原子半径はピコメートル(pm)で測定され、メートルの倍数です(1ピコメートル= 10-12 m。)。 参照が原子ではなくイオンである場合、検出される半径はイオン半径であることに注意してください。
原子半径の変動
周期表では、原子半径の成長は次の図で見ることができます:
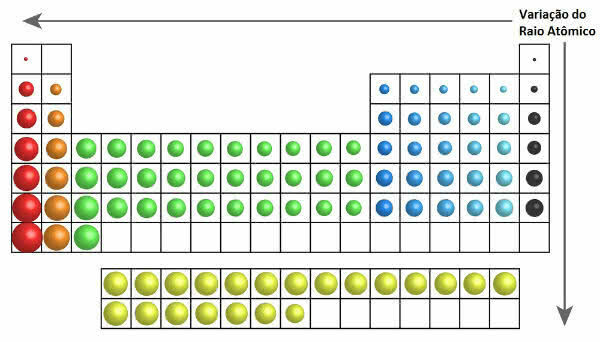 周期表の原子半径の変化
周期表の原子半径の変化
したがって、垂直方向(ファミリまたはグループ)の原子半径は上から下に向かって増加します。 水平(周期)では、右から左に増加します。
の逆変化を参照してください 電子親和力 そして 電気陰性度.
イオン化エネルギー
THE イオン化エネルギー(またはポテンシャル) これは、電子をシフトするために必要なエネルギーを決定する周期特性でもあり、電子ボルト(eV)で表されます。
あまりにも読んでください: 周期表.
コメント付きの解決策で入試の質問を確認してください: 周期表の練習.


