幾何学的な電子分布 を表す別の方法です 基本的な電子配信 原子の、つまり、一般的に実行される原子の ライナス・ポーリングのエネルギー図.
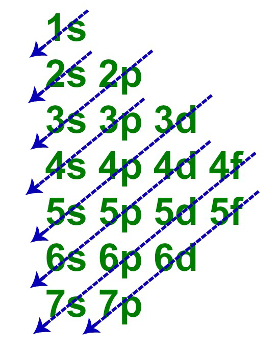
矢印がエネルギーの順序を示すライナス・ポーリング図
したがって、幾何学的な電子分布の構築は、基本的な分布の実現に依存することを強調する必要があります。 それらの違いは次のとおりです。
幾何分布は常に1本の線で表されます。
幾何分布は次の順序に従いません(青い矢印)ライナス・ポーリング図によって実行されるエネルギーの;
基本的な分布は1本の線で表すことができますが、常に図のエネルギー順序に従う必要があります。
どのように理解するには 幾何学的な電子分布、元素亜鉛を使用しましょう(原子番号 30)次の手順の例として:
最初のステップ: 30を配布します 電子 原子番号を参照します。
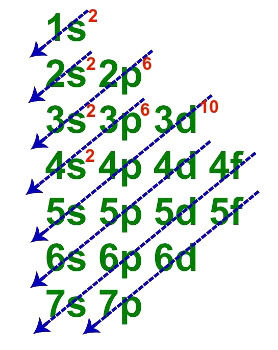
亜鉛の基本的な電子配信
2番目のステップ: ダイアグラムの各線(1、2、3、および4)を表す線に幾何分布を作成します。
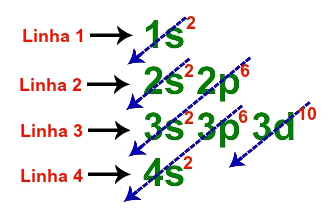
亜鉛の基本的な分布に使用される線
亜鉛の基本分布の4つの線は、次のように幾何分布で表されます。
亜鉛の幾何分布:1秒2 2秒2 2p6 3秒2 3p6 3D10 4秒2
幾何学的な電子分布の特徴
アトムの最も外側のサブレベルを決定します。
陽イオンを形成する傾向のある原子内の電子吸引の位置を決定します。
陰イオンを形成する傾向がある原子内の電子吸引の位置を決定します。
幾何学的な電子分布の例
最初の例: ウラン元素(Z = 92)
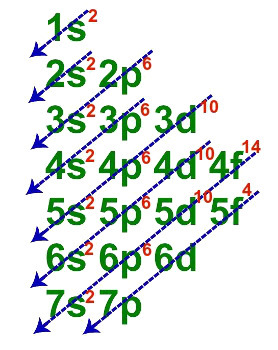
ウラン元素の電子的分布
ウランの基本的な電子分配には、次の説明のように、合計7つのラインがあります。
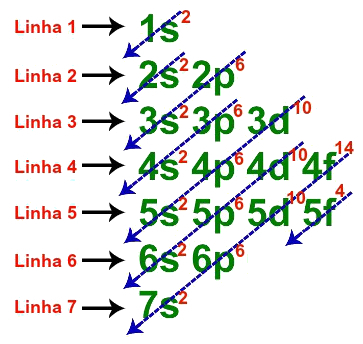
ウランの基本的な分布に使用される線
7つの線のそれぞれが単一の線で表される場合、ウランの幾何学的な電子分布は次のように表されます。
1秒2 2秒2 2p6 3秒2 3p6 3D10 4秒2 4p6 4d10 4f14 5秒2 5p6 5d10 5f4 6秒2 6p6
2番目の例: セシウム元素(Z = 55)
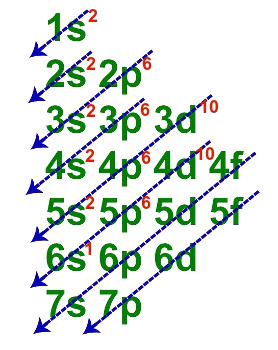
元素セシウムの電子配布
セシウムの基本的な電子配布には、次の説明のように、合計7つの行があります。
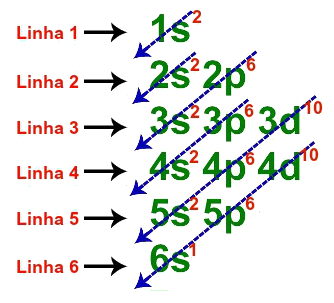
セシウムの基本的な分布に使用される線
6本の線のそれぞれが1本の線で表される場合、セシウムの電子幾何分布は次のように表されます。
1秒2 2秒2 2p6 3秒2 3p6 3D10 4秒2 4p6 4d10 5秒2 5p6 6秒1
私によって。DiogoLopesDias
ソース: ブラジルの学校- https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-distribuicao-eletronica-geometrica.htm
