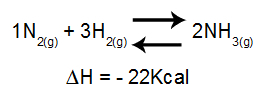“化学結合」は、1920年にギルバート・ニュートン・ルイスがその理由を説明する記事で最初に使用した用語でした。 その原子は互いにくっついて物質を形成し、なぜそれらは何千もの原子がくっつくのか 年歳。
これまでに知られ、周期表に記載されているほとんどの化学元素の原子は、自然界では孤立した形で現れません。 私たちの日常生活に存在する物質のほとんどは、単純な(原子からなる)物質です。 1種類の化学元素のみ)または複合材料(2つ以上の化学元素の原子を含む) 多くの異なる)。
これは、原子が他の原子と化学結合を形成する能力を持っているためです。他の原子は、同じ元素でも異なる元素でもかまいません。 これらの結合は非常に強力であるため、外部からの影響がなくても、ほとんどの場合、原子はそのまま結合されたままになります。
マインドマップ:化学結合

*マインドマップをPDFでダウンロードするには、 ここをクリック!
たとえば、自然界で遊離酸素原子を見つけることは一般的ではありません。 しかし、他の原子に付着しているように見える物質がいくつか見つかります。 単体の例は、各分子が2つの結合した酸素原子(O2); 一方、複合物質の例は水であり、各分子には2つの水素原子が酸素原子(H2O)。
自然界で安定して隔離されていることがわかっている唯一の要素は、 希ガスつまり、周期表のファミリー18の元素(He、Ne、Ar、Kr、Xe、Rn)です。 これらすべての元素は、ヘリウム(He)を除いて、最後の電子殻(原子価層)に8つの電子を持っているという共通の事実を持っています。 これは、電子殻(K層)が1つしかないため、2つの電子を保持します。これは、その中で可能な最大の電子数です。 層。
したがって、ギルバートN。 ルイスと科学者のウォーターコッセルは、 他の元素の原子は結合して8個の電子(Kシェルしかない場合は2個)を持ち、安定します。 だから、 原子価の電子理論、説明されたアイデアに基づいて、元素の原子が作る化学結合の数を示します。
今やめないで... 広告の後にもっとあります;)
したがって、 原子は化学結合を形成し、次の希ガスの配置に到達するまで価電子を失ったり、獲得したり、共有したりしようとします。この理論も呼ばれるようになりました オクテット則.
たとえば、酸素は価電子殻に6つの電子があるため、2価です。 したがって、希ガスネオン(Ne)の構成を持つには、さらに2つの電子を受け取る必要があります。つまり、価電子シェル(この場合はLシェル)に8つの電子があります。 上記の酸素ガスと水の場合、次のようになります。
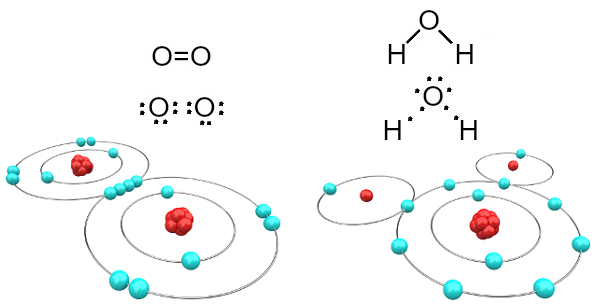
共有結合によって形成される酸素と水分子
最初のケースでは(酸素ガス-O2)、各酸素原子は2つの電子を共有し、どちらも価電子シェルに8つの電子を持っています。 これは、 二重結合 (2つの原子間で同時に2つの結合)。
水の場合、2つの水素原子のそれぞれが中央の酸素原子と電子を共有し、 すべてが安定しています(酸素は価電子シェルに8つの電子を持ち、各水素は2つあります 電子)。 ここでも2つの簡単な接続が行われます。
すべての原子が電子(水素、非金属、半金属)を受け取る必要があり、電子がペアで共有されるこのタイプの化学結合は、と呼ばれます。 共有結合。
しかし、化学結合にはさらに2つのタイプがあります。
(1) イオン結合 →ある原子から別の原子への電子の決定的な移動があります。 このタイプの結合は、金属原子間で発生します(電子を失って留まる傾向があります) 安定)および水素原子、非金属および半金属(電子を獲得して留まる傾向がある) 安定)。
例としては、塩化ナトリウム(NaCl-食卓塩)があります。ナトリウムは電子を失う傾向がある金属であり、塩素は電子を得る傾向がある非金属です。 したがって、ナトリウムは寄付します(赤い矢)電子から塩素へ、非常に安定した物質である塩を形成します。 彼らは卒業するので (黒い矢印) 反対の電荷を持つ化学種であるイオン (+ そして -)、1つのイオンが近くの別のイオンを引き付け、食卓塩の結晶と同様に、イオンクラスターが膨大な数のイオンで形成されます。

イオン結合による塩化ナトリウムの形成
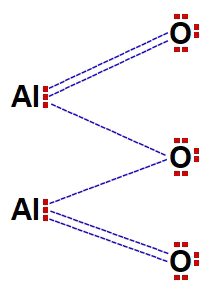
(2) 金属接続 →金属(アルミニウム、金、銀、銅など)は中性子原子のクラスターによって形成され、 自由電子(陽イオンの形成で失われた電子)の一種の「雲」によって一緒に保持されている陽イオン 引用)。 この電子の雲(または海)は、原子をまとめる金属結合として機能します。
これらのタイプの化学結合とオクテット則の詳細については、以下の関連記事を参照してください。
M.eビクターリカルドフェレイラによるマインドマップ
化学の先生
ジェニファー・フォガサ
化学を卒業
化学
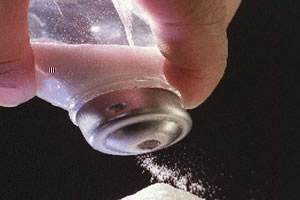
イオン結合、イオン性化合物、イオン性凝集物、塩化ナトリウム、食卓塩、イオン性物質間の配置、 静電引力、塩化物陰イオン、ナトリウム陽イオン、極性溶媒、陽イオン、陽イオン、陰イオン、 陰イオン。