O 硝酸アンモニウム 分子式NHの固体物質です4で3 と白い外観(純粋な場合)。 構成 によって イオン NH4+ (アンモニウム)およびNO3- (硝酸塩)、可燃性ではありませんが、酸化性が高く、反応性があります。 その分解反応により、生成物として大量のガスが発生し、爆発の恐れがあり、この生成物の不適切な保管が深刻な問題となります。 そしてまた 農業で広く使用されています 肥料として。
あまりにも読んでください: 天然物質-自然に由来する分子
硝酸アンモニウムとは何ですか?

硝酸アンモニウム それは塩です NHイオンで構成4+ (アンモニウム)およびNO3- (硝酸塩)。 それは固体の化合物であり、 純粋なとき, 色は白です。 農業用肥料として広く使用されていますが、爆発物の製造にも使用できます。 それは非常に酸化性の物質です、次に酸化します。 硝酸アンモニウムの暴走反応は、 ガス、原因 爆発性の影響.
今やめないで... 広告の後にもっとあります;)
硝酸アンモニウムの特性
モル質量:80.04336g / mol。
イオンで構成される塩:アンモニウム(NH4+)および硝酸塩(NO3-).
外観:白い固体。
強い酸化性です。
他の物質と簡単に反応します。
可燃性ではありません。
通常の温度および圧力条件の場合:
-密度:1.73g /cm³;
-沸点:210°C;
-融点:169.6°C;
-水への溶解度:216 g / 100ml;
-pH:5.5(0.2M)。
硝酸アンモニウム式
この化合物の分子式はNHです4で3.
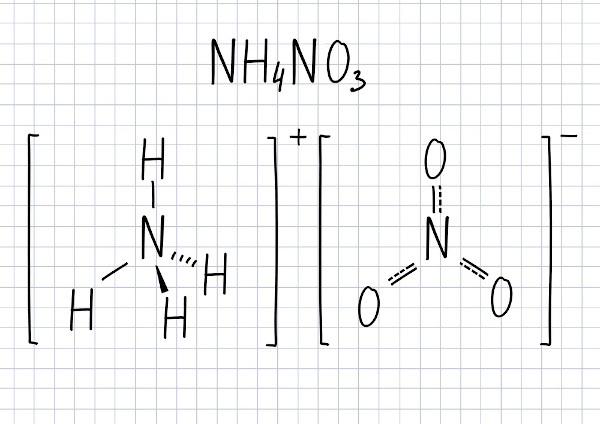
硝酸アンモニウムの分解
であるために 反応性が高く、酸化電位が高い物質、 硝酸アンモニウムは、高温にさらされると、 分解反応、主な製品はガス、窒素、 酸素 と水蒸気。 分解は2つのステップで行われます。
→ 最初のステップ:
2NH4で3 (s)→2N2O(g)+ 4H2O(g)
→ 第2段階:
2N2O→2N2(g)+ O2(g)
→ グローバル方程式:
2NH4で3 (s)→2N2(g)+ O2(g)+ 4H2O(g)
最初の式では、製品の1つ 分解で得られるのは 亜酸化窒素(N2O)、 としても知られている 笑気. これは、主に歯科医によって、燃料を燃焼させるための自動車エンジンの出力を高めるために、また麻酔薬として使用されます。 も 責任がある主なガスの1つ 温室効果.
も参照してください: 化学反応の種類は何ですか?
硝酸アンモニウムの生産
硝酸アンモニウムは次の方法で入手できます。 硫酸アンモニウム(NH4)間の反応2のみ4 および硝酸カルシウムCa(NO3)2. 下記参照:
(NH4)2のみ4 + Ca(NO3)2 → 2 NH4で3+ケース4
ガス状アンモニアからも製造できます、これは硝酸溶液中で泡立たせられ、反応生成物として硝酸アンモニウム水溶液を有する。 見てください:
NH3(g) + HNO3(aq) → NH4で3(ここに)
硝酸アンモニウムの使用

- 肥料製造
- 鉱山、採石場、建設現場での爆発物
- 除草剤と殺虫剤
- 工業用途向けの亜酸化窒素の入手
- 酸化物の吸収剤
- ロケット推進剤用の酸化剤
- 等温バッグの製造
- 養蜂におけるじんましんの管理のための麻酔煙の生成
また、アクセス: 火と戦う方法は?
硝酸アンモニウムの危険性
硝酸アンモニウムに関連する主なリスクの1つは 不十分な保管. それは非常に酸化性の物質であり、他のいくつかの化合物と反応するため、 大量のガスの放出との反応. 不適切な保管は、可燃性製品による汚染、熱またはガスの保持への暴露の影響を受けます。 爆発を引き起こす可能性のあるもの.
これは、たとえば米国のテキサス州で、2,086トンの硝酸アンモニウムを運ぶフランスからの貨物船ですでに起こっています。 事故が起こった 1947年 そしてテキサスシティ災害として知られるようになりました。 悲劇は581人の死を引き起こしました そして、それは、アンモニウム貨物に到達した船に含まれていない火災が原因で発生し、爆発を引き起こしました。
別の例は 爆発シーケンス 2020年8月4日に港で起こった レバノン、ベイルート市 100人以上が死亡し、5,000人が負傷した。 爆発の大きさは、そこに貯蔵された2,750トンの硝酸アンモニウムの貨物の連鎖反応の発火によるものでした。
硝酸アンモニウムが引き起こす可能性があることも注目に値します 皮膚および眼の刺激 そして、吸入された場合、 呼吸の問題. 血流中の物質は体液と反応するため毒性があり、硝酸塩などのこの反応の生成物は健康に害を及ぼす可能性があります。 青色児病、 乳児メトヘモグロビン血症(低血中ヘモグロビン)としても知られています。 この病気は、農業地域の水域の肥料に存在する硝酸アンモニウムによる汚染のために、農村地域の家族に再発しています。
LaysaBernardes著
化学の先生
学校や学業でこのテキストを参照しますか? 見てください:
ARAúJO、Laysa Bernardes Marquesde。 "硝酸アンモニウム"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/nitrato-de-amonio.htm. 2021年6月27日にアクセス。
生物学
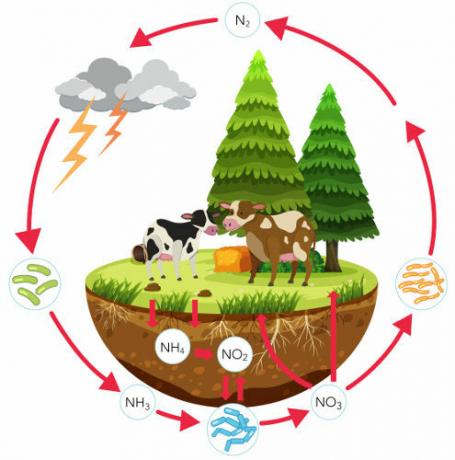
この元素の循環を確実にする重要な生物地球化学的循環である窒素循環についてもっと学びましょう。 このテキストでは、窒素循環の各ステップに取り組み、その重要性について説明し、このプロセスにおける細菌の役割に焦点を当てます。 また、このテーマに関する演習も行います。