にちなんで名付けられた要素 アルカリ土類金属 周期表のファミリー2またはIIAに属するものです。 このようなグループには、次の化学元素が含まれます。 Be(ベリリウム)、Mg(マグネシウム)、Ca(カルシウム)、Sr(ストロンチウム)、Ba(バリウム)、ラジウム(Ra)。

それらは価電子殻に2つの電子を持ち、それらの一般的な分布はns2で表されます。 番号 最後のレベルの番号を表します。 この特性により、これらの2つの電子を失う傾向があり、2 +の電荷カチオンが発生します。
「地球」という用語は、これらの元素が主に鉱物に見られる場所であるため、「地球上に存在する」を指します。 例えば、リン酸カルシウム化合物(Ca3(ほこり4)2)、地球の地殻に含まれ、リンの生産の原料として機能します。 動物の骨にも多く含まれているため、これらを煆焼すると、リン酸カルシウムを含むいわゆる「骨粉」が得られます。
アルカリ土類金属の中で最も目立つのは カルシウム それは マグネシウム.
- カルシウム
カルシウムイオン(Ca2+)私たちの骨と歯の約90%に存在します。 そして動物ではそれは彼らの殻にも存在します。 その機能は、骨の構造を強化し、筋弛緩薬として機能することです。 体内のカルシウムが不足すると、筋肉のけいれん、破傷風、骨粗鬆症を引き起こす可能性があります。 そのため、ミルクとその派生物(バター、チーズなど)、肉、野菜など、カルシウムが豊富な食品を通して食べることが重要です。
一方、カルシウムが多すぎると、筋肉の弛緩、腎臓結石、骨の痛みを引き起こす可能性があります。
前述の食品に加えて、カルシウムは自然の多くの部分、特に方解石(CaCO)などのミネラルにまだ存在しています3)または石灰岩と大理石の成分である炭酸カルシウム、および大理石は流し、彫像、床および階段の製造に使用されます。 炭酸カルシウムは、洞窟内の鍾乳石や石筍の生成物でもあります。 カルシウムは天然石膏(CaSO)にも含まれています4. 2時間2O)、石膏と呼ばれます。 この塩は脱水することができ、CaSOを生じます4 学校のチョークである無水。
今やめないで... 広告の後にもっとあります;)
産業界では、バージンライム(CaO)が製造されます。これは、消石灰または消石灰とも呼ばれ、実際には水酸化カルシウム(Ca(OH))です。2)、しっくい塗料やモルタルの調製に使用されます。 石膏を穏やかに加熱することで、建設に使用される石膏である半水和硫酸カルシウムを得ることができます。 市民社会、以下に示す腕の骨折のような骨折を保護するための歯科および医学におけるカビの製造。
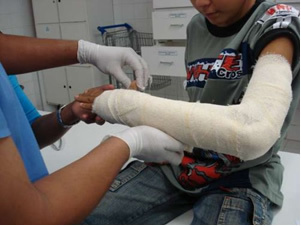
- マグネシウム
のイオン マグネシウム また、骨の70%に存在し、酵素、筋肉、運動協調性の作用を促進するため、生物学的にも非常に重要です。 体の欠如は、見当識障害、高血圧、震え、および弱い脈拍を引き起こす可能性があります。 したがって、この要素を含む次の食品を食べる必要があります:ナッツ、穀物、緑の野菜。 また、体内の過剰なマグネシウムは眠気を引き起こす可能性があります。
マグネシウムは海水やミネラルにも含まれています。 犠牲金属(鋼の代わりに酸化して腐食を防ぐ)などの金属合金、「マグネシウム」ホイール、花火(銀と白の色を提供)で使用されます。 マグネシウムの非常に重要な化合物は水酸化マグネシウム(Mg(OH)2)、これは、水に分散すると、約7%の濃度で、既知の懸濁液を生じます。 制酸剤として働き、胃の酸性度(胸焼け)と戦うマグネシアのミルクとして、そして 下剤。

ジェニファー・フォガサ
化学を卒業
