
カロリーの量は、食品の構成によって異なります。 したがって、食品から放出され、体に吸収される熱の量を実験的に決定するために、私たちはと呼ばれる装置を使用します 熱量計.
この装置は、食品が燃焼したときに食品から放出される熱を測定します。 熱量計にはいくつかの種類があります。 それらの最初のものは1780年にラヴォワジエとラプラスによって作成され、 氷熱量計.
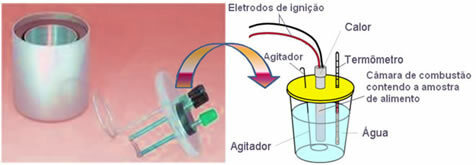
今日、最も使用されており、上で説明したカロリーの概念を考慮に入れているのは、 水熱量計. このデバイスは、媒体からの熱損失を防ぐために絶縁材料でコーティングされています。 分析対象の食品は 燃焼室、酸素ガスを含み、 電極. これらの電極は放電を受け、食品の発火と燃焼を引き起こします。
熱量計に含まれる既知の水分量は、燃焼した食品から放出される熱を吸収し、 温度計 水温の上昇を測定します。 さらに、熱量計には アジテーター これにより、水温が全体を通して均一に保たれます。
たとえば、1グラムの砂糖の質量を使用し、熱量計に1000 gの水がある場合、最終的にそれを観察します。 反応の水温は20°Cから24°Cになりました。つまり、4°C上昇すると、次のエネルギー値に達することができます。 シュガー。 お気に入り? さて、最初のカロリーの概念を考えると、次のようになります。
| 1°Cから上げる→水1グラムあたり1カロリー |
| 4°Cから上げる→水1グラムあたり4カロリー |
したがって、1gの水が4つの石灰を吸収します。 ただし、1000 gの水を使用し、燃焼で放出される熱がすべて吸収されることを考慮すると、水が吸収する総エネルギーは4000calまたは4kcalでした。 したがって、次のように結論付けます。
今やめないで... 広告の後にもっとあります;)
| 砂糖のエネルギー値= 4000 cal / gまたは4kcal / g。 |
SIへの変換:
1 kcal 4.18 kJ
4 kcal / g x
x = 16.72 kJ / g
さらに、次の式を使用して、水によって放出または吸収される熱量を計算できます。
| Q = m。 ç。 t |
どこ:
Q =水によって放棄または吸収された熱。
m =水の質量;
c =水の比熱。1.0cal/ gに相当します。 °Cまたは4.18J / g。 °C;
Δt=水が受ける温度の変化。これは、最初の温度による最終温度の低下によって与えられます(tf – t私).
この式を使用すると、同じ結果が得られます。
Q = m。 ç。 t
Q = 1000g。 1.0カロリー/ g。 °C。 (24-20)°C
Q = 4000カロリー
Q = 4.0 kcal
または
Q = m。 ç。 t
Q = 1000g。 4.18 kJ / g °C。 (24-20)°C
Q = 16.72 kJ
ジェニファー・フォガサ
化学を卒業
学校や学業でこのテキストを参照しますか? 見てください:
FOGAÇA、ジェニファー・ロシャ・バルガス。 "熱量計を使用した食品カロリーの測定"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/medindo-as-calorias-dos-alimentos-por-meio-um-calorimetro.htm. 2021年6月27日にアクセス。


