で 分子間力 確かに、国立高校の試験に現れることができる化学のトピックです(そしてどちらか). したがって、この記事でこの主題の主な内容を確認する価値があります。
定義
分子間力 それらは、さまざまな強度(弱い、中程度、または強い)の力であり、静電引力または物質の分子間に確立された結合によって、それらの間の結合を維持します。
分子間力の種類
) 誘導双極子
そしてその 分子間力 これは、無極性の特性を持つ物質の分子間で発生します。 たとえば、Oなどの物質の分子間で発生します2、H2、 番号2、CO2、CH4.
これらの分子間の結合は、それらの間に双極子が作成されるときに発生します。 これは、ある分子からの電子が別の分子からの電子を置き換えて、ある分子から別の分子に移動する負と正の極を作成するときに発生します。
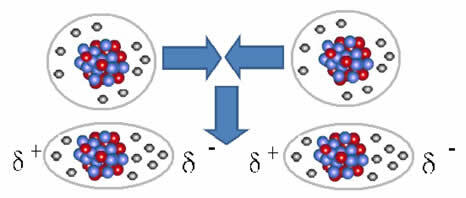
非極性分子における双極子形成の表現
これらの分子の間に2つの極が形成され、一方の負極が他方の正極と相互作用します。 これらの極が作成されたため、それは低強度の分子間力です。
B) 永久双極子
そしてその 分子間力 これは、極性特性を持つ物質の分子間で発生します。 例としては、HCN、Hなどの物質の分子があります。2O、NH3、CO、CH3Cl。
これらの分子間の結合は、一方の負極が他方の正極と相互作用するときに発生します。
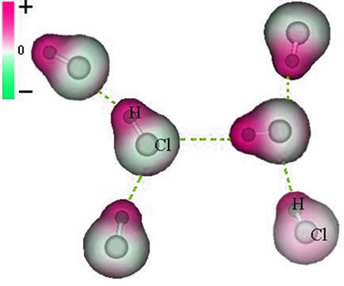
HCl分子間の永久双極子力の表現
極がすでに存在するため、永久双極子分子間力は、誘導双極子よりも強度が大きくなります。
ç) 水素結合
それ 分子間力 これは、水素原子が酸素、窒素、またはフッ素原子に直接結合している極性分子間で発生します。
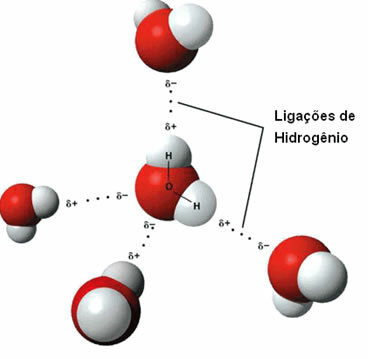
水分子間の水素結合の表現
水素結合は、一方の分子の水素がもう一方の分子の酸素、窒素、またはフッ素と相互作用するときに形成されます。
d)双極子イオン
この分子間力は、非結合性電子のペアを持つ極性分子と、溶液中のイオン(陽イオンまたは陰イオン)の間で発生します。
たとえば、水分子には、酸素中に2対の非結合電子があります。 水性媒体にイオンがある場合、その中に極があるため、それらは水分子に近づきます。
今やめないで... 広告の後にもっとあります;)
重要性
を知ることの重要性 エネムの分子間力 それは、物質の物理的状態、融点、沸点、および溶解度に関して彼らがもたらす理解です。
) 物質の融点と沸点との関係
融点は固体から液体状態への遷移の温度を示し、沸点は液体から気体状態への遷移の温度を示します。
ある物理的状態を別の物理的状態と区別するのはその分子間の凝集のレベルであるため、このパッセージは物質の分子間の相互作用に直接関係しています。
したがって、分子間力が強いほど、融点と沸点が高くなります。 分子間力が弱いほど、融点と沸点は低くなります。 したがって、融点と沸点の降順を定義できます。
水素結合>永久双極子>誘導双極子
B) 溶解度との関係
一般に、likeはlikeを溶解します。つまり、極性物質は極性物質を溶解し、非極性物質は非極性物質を溶解します。
ただし、溶質分子と溶媒分子の間の相互作用の可能性はまだあります。 これは、この新しい相互作用が物質自体の分子間にすでに存在するものよりも大きい場合にのみ発生します。
エネムにおける分子間力の適用例
最初の例: (Enem-2011)人間の皮膚は、十分に水分を補給すると、優れた弾力性と柔らかく滑らかな外観を獲得します。 一方、乾燥すると弾力性が失われ、不透明でざらざらした感じになります。 皮膚の乾燥を防ぐために、可能な限り、一般的にグリセリンとポリエチレングリコールから作られた保湿保湿剤を使用する必要があります。

保湿剤によって促進される皮膚表面の水分保持は、湿潤剤のヒドロキシル基と環境に含まれる水分との相互作用の結果です。
a)イオン結合
b)ロンドン力
c)共有結合
d)双極子-双極子力
e)水素結合
水分子は酸素原子に水素結合しているため、この質問に対する答えは水素結合です。 同じことがプロピレングリコールとポリエチレングリコールの分子でも起こります。これは、このタイプの分子間力が発生するための好ましい条件です。
私によって。DiogoLopesDias
学校や学業でこのテキストを参照しますか? 見てください:
DAYS、ディオゴロペス。 "エネムの分子間力"; ブラジルの学校. で利用可能: https://brasilescola.uol.com.br/quimica/forca-intermoleculares-no-enem.htm. 2021年6月27日にアクセス。