ה גשר מלח הוצע על ידי הכימאי האנגלי פרדריק דניאל, בשנת 1836, כאשר חוקר זה הקים את סוֹלְלָה נקרא על שמו (ערימת דניל). הגשר הזה הוא צינור בצורת U בעל שני קצוות נקבוביים. (מורכב מכותנה או אגר-אגר) ומכיל תמיסה מימית שנוצרת על ידי מים ומלח. הוא מחבר בעקיפין את הפתרונות של שני תאי החצי של התא (האנודה והקטודה).
תַצְפִּית: האנודה היא הקוטב השלילי של הסוללה והיא המקום בו מתרחשת חמצון, והקטודה היא הקוטב החיובי ושם מתרחשת הפחתה.
על מנת להבין את חשיבות גשר המלח, יש צורך בהתחלה להבין כיצד פועלת הערימה. ראה את התרשים להלן:
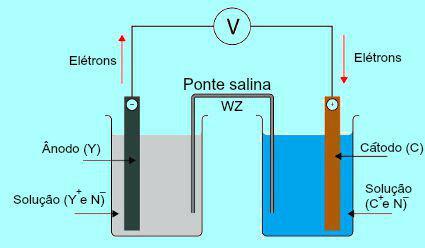
ערכה כללית של ערמת דניאל
בתחילה, המתכת (Y) של הלוח המצוי באנודה עוברת חמצון. כאשר עוברים חמצון, המתכת הופכת לקטיון, הנופל לתמיסה בה נמצאת הפלטה. מסיבה זו, תמיסת האנודה מתחילה להציג ריכוז גבוה יותר של קטיונים (Y+). במקרה זה, נצפתה ירידה בלוחית מתכת האנודה.
Y → ו- + Y+
לאחר מכן, האלקטרונים שאבדו במהלך חמצון המתכת של לוח האנודה עוברים דרך חוט החשמל החיצוני ועוברים אל לוחית המתכת הקיימת בקתודה. לפיכך, הלוח הקיים בקתודה טעון אלקטרונים.
-
הקטיונים הנוכחיים (ג+) בתמיסה לנוע לכיוון לוח הקתודה מכיוון שהיא טעונה באלקטרונים. הקטיונים, כאשר הם צוברים את האלקטרונים הקיימים בלוח, הופכים לניטראליים (יציבים ומוצקים) ונצמדים אליה. מסיבה זו, תמיסת הקתודה מציגה ריכוז גבוה יותר של אניונים מאשר של קטיונים. במקרה זה, נצפתה עלייה בגודל לוחית המתכת הקתודית.
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
Ç+ + ו- → ג
מתוך ההבנה כיצד ה ערימתו של דניאל, ניתן לראות כי הפתרון הקיים באנודה מקבל כמות גדולה יותר של קטיוניות Y+ בגלל החמצון של המתכת של לוח X. לעומת זאת, התמיסה הקיימת בקתודה מאבדת את הקטיונים שלה (C+) מכיוון שהם סובלים מהפחתה ברובד.
בדיוק בנושא זה מודגשת עבודת גשר המלח. תפקידו העיקרי של גשר זה הוא לקדם את איזון המטענים הקיים בתמיסות האנודה והקטודה. בגשר המלח, תמיד יש לנו מלח (בדרך כלל אשלגן כלורי או אמוניום חנקתי.) המנותק במים. ראה ייצוג של משוואה בגשר המלח:
WZ + H2O → W+ + Z-
בגשר המלח ישנם שני יונים (W+ ו- Z-), המועברים לקתודה ולאנודה על פי:
ה) האנודה מקבלת את האניונים (Z-) הנמצא בגשר המלח עקב חמצון היסוד (Y), הגורם לעלייה בכמות הקטיונים (Y+) בפתרון.
ב) הקתודה מקבלת קטיונים (W+) של גשר המלח מכיוון שבמהלך הפעלת הסוללה הקטיון (C+) הקיים בפתרון מצטמצם על הלוח. לפיכך, לתמיסת הקתודה יש כמות גדולה יותר של אניונים (N-) ולכן מקבל את הקטיון שנמצא בגשר המלח.
על ידי. דיוגו לופס דיאס
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
DAYS, דיוגו לופס. "גשר מפרש"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/ponte-salina.htm. גישה אליו ב -28 ביוני 2021.
