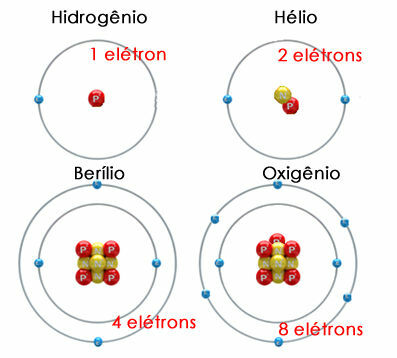
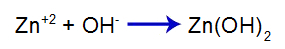
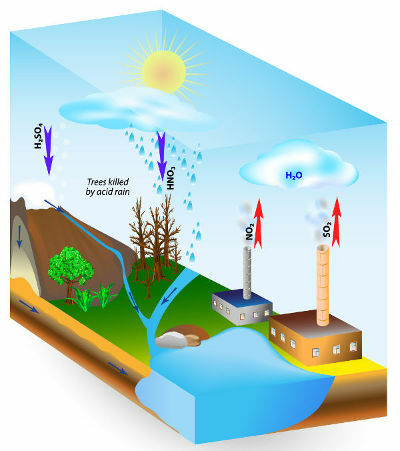
כשאנחנו מדברים על pH, אנו מתייחסים לפוטנציאל ההידרוגניוני של תמיסה, כלומר לכמות הקטיונים ההידרוניום (H+ או H3או+) המפוזרים בממיס של תמיסה.
קטיונים של הידרוניום ידועים היטב בגלל ההגדרה שהציע המדען ארניוס לחומצה. מדען זה טוען כי חוּמצָה האם כל חומר מסוגל ליינן ומייצרים יוני הידרוניום במדיום מימי.
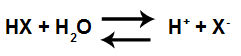
משוואת יינון חומציות
ראשי התיבות pH משמש כנקודת התייחסות לקביעת רמת החומציות של מדיום. אבל במשך זמן רב, כימאים השתמשו גם ב pH כהתייחסות לקביעת, בנוסף לחומציות, אם מדיום הוא בסיסי או ניטרלי.
זה אפשרי מכיוון שכימאים מודעים כעת לכך שמים עוברים יינון עצמי, כלומר הם מייצרים הידרוניומים (H+) והידרוקסידים (OH-). לפיכך, בתמיסה מימית לעולם אין רק הידרוניום או הידרוקסיד, אלא שניהם, כפי שניתן לראות מהמשוואה הבאה:

משוואת אוטומציה של מים
ערכים המשמשים כנקודת התייחסות ל- pH
הערכים המשמשים עבור pH מתייחסים לקבוע יינון (Kw) של מים בטמפרטורה של 25אוC, ששווה ל- 10-14. בטמפרטורה זו, ריכוזי הידרוניום והידרוקסיד המופקים על ידי מים שווים לחלוטין, כלומר 10-7 פְּרוּצָה.
[ח+] = [אה-]= 10-7
מתוך התייחסות זו, הערכים המשמשים ל- pH נעים בין 0 ל -14.
נוסחאות לחישוב ה- pH
א) חישוב מהריכוז במול / ליטר של קטיונים הידרוניום
חישוב ערך ה- pH יכול להיעשות ישירות, כל עוד אנו יודעים את ריכוז ההידרוניומים ([H+]). תראה:
pH = -לוג [H+]
אוֹ
10-pH = [ח+]
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
ב) חישוב מריכוז אניוני הידרוקסיד (OH-)
pOH = -log [OH-]
אוֹ
10-POH = [אה-]
לאחר חישוב ערך ה- pOH, עליך להשתמש בו בביטוי הבא כדי לקבוע את ערך ה- pH.
pH + pOH = 14
פרשנות של ערכי pH
בידיעת ערך ה- pH, אנו יכולים לקבוע אם לתמיסה המדוברת אופי חומצי, בסיסי או ניטרלי. לשם כך פשוט השתמש בקשר הסכמטי הבא:
לערכי pH מתחת ל 7 = מדיום חומצי;
עבור pH עם ערך השווה 7 = מדיום ניטרלי;
לערכי pH מעל 7 = מדיום בסיסי.
דוגמאות
דוגמה ראשונה: בידיעה שריכוז קטיונים של הידרוניום בתמיסה הוא 2.10-4 mol / L, מה צריך להיות ערך ה- pH של תמיסה זו?
לקביעת ערך ה- pH של התמיסה מריכוז הידרוניומים (H+), 2.10-4 mol / L, עלינו להשתמש בביטוי הבא:
pH = -לוג [H+]
pH = -לוג [2.10-4 ]
pH = - (יומן 2 + יומן 10-4)
pH = -log2 - log10-4
pH = –לוג 2 - 4. לוג 10
pH = –0.3 + 4. (1)
pH = -0.3 + 4
pH = 3.7
דוגמה שנייה: לתמיסה שנוצרת על ידי מומס מסוים יש ריכוז יונים של הידרוקסיד שווה ל -10-11 פְּרוּצָה. מריכוז זה, אנו יכולים לומר כי ה- pH של פתרון זה שווה כמה?
לקביעת ערך ה- pH של התמיסה מריכוז ההידרוקסיד, 10-11 mol / L, עלינו לעשות את הפעולות הבאות:
1או שלב: לחשב את ערך ה- pOH.
10-POH = [אה-]
10-POH = 10-11
עלינו להכפיל את הביטוי ב -1 מכיוון ש- pOH הוא תמיד לא ידוע חיובי.
-pOH = -11. (- 1)
pOH = 11
2או שלב: לחשב את ערך ה- pH.
pH + pOH = 14
pH + 11 = 14
pH = 14 - 11
pH = 3
על ידי. דיוגו לופס דיאס
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
DAYS, דיוגו לופס. "מה זה pH?"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-ph.htm. גישה אליו ב -27 ביוני 2021.
כִּימִיָה
מינרל הידרוקסיפטיט, pH בפה, עששת, קורוזיה בשיניים, יישום תקופתי של פלואוריד, בריאות הפה, o עישון ושיניים, כתמי שיניים, סרטן שפתיים, חומצה הידרוכלורית, בולימיה, חומצה לקטית, ספוג, סיל