או עִקָרוֹןנותןחוסר ודאות, נקרא גם עקרון אי הוודאות של הייזנברג 1927, על ידי הפיזיקאי הגרמני ורנרהייזנברג (1901-1976). עיקרון זה מצביע על כך שלא ניתן למדוד, בּוֹ זְמַנִית ועם דיוק, כמויות הקשורות ישירות, כגון מְהִירוּת ו עמדה של גוף.
תראהגַם: היבטים של תורת הקוונטים
סיכום עקרון אי וודאות
עקרון אי הוודאות מתייחס לשני כמויות, כגון מיקום ומומנטום או אנרגיה וזמן, דרך תוצר חוסר הוודאות של המדידות שבוצעו בהם.
על פי עקרון חוסר הוודאות, ככל שמיקום הגוף מדויק יותר, כך מדידת המומנטום שלו מדויקת פחות.
עקרון אי הוודאות קובע כי לא ניתן לדעת, בדיוק מלא ובו זמנית, שתי כמויות פיזיקליות קשורות, הנקראות גם כמויות מצומדות קנונית.
מהו עקרון אי-הוודאות של הייזנברג?
או עקרון אי הוודאות של הייזנברג היא תוצאה תיאורטית מוזרה המתקבלת באמצעות חישובים בתחום מכניקה קוואנטית, שהבסיס שלו הוא בדיוק העיקרון הזה. באמצעות הידע בפיזיקה קלאסית, האמינו כי, לדעת את מיקום ההתחלה ואת המהירות, יותר באופן ספציפי את כמות התנועה, של גוף או מערכת של גופים, ניתן יהיה לחזות את התנהגותו ב רגעים עתידיים. באופן זה ניתן יהיה לחשב עמדות מאוחר יותר, קביעת שלה
מַסלוּל, ערכים של תְאוּצָה,מְהִירוּת,אֵנֶרְגִיָה, וכו ' עם זאת, עקרון אי הוודאות מראה שגם אם היה לנו את יותרנחוץ ממכשירי המדידה בהישג יד, לא נוכל לדעת, בּוֹ זְמַנִית ועם דיוק, גדלות כמו עמדה ו הכמותבתנועה אואֵנֶרְגִיָה ו לשבורבזְמַן של אותו גוף.תראהגַם: כמות תנועה
אז, על פי עיקרון זה, אם נוכל לקבוע את עמדה של גוף עם דיוק מוחלט, נאבד לחלוטין את המידה שלו הכמותבתְנוּעָה, מכיוון שהאי-דיוק לגביה ייחשב אינסופי. כמו כן, אם נוכל להיות בטוחים לגבי כמות התנועה של הגוף, לא ניתן יהיה לדעת את מיקומו.
כנ"ל לגבי הגדולים אֵנֶרְגִיָה ו זְמַן: אם אנו יודעים בדיוק את כמות האנרגיה בחלקיק, נאבד דיוק במדידות הזמן. כמו כן, אם נדע כמה זמן לקח לאירוע להתרחש עם חלקיק מסוים, היינו מאבדים לגמרי מידע על כמות האנרגיה הקיימת בו.

בגלל עקרון אי הוודאות, אי אפשר שרמת האנרגיה הנמוכה ביותר בגוף תהיה אפס.
תראהגַם: מהי אנרגיה?
לא כל הכמויות הפיזיות קשורות זו לזו בגלל מידת הדיוק שלהן. אפשר, למשל, לקבוע את אֵנֶרְגִיָה וה עמדה של חלקיק בלי שדיוק המדידות הללו יהיה בְּיַחַס הָפוּךיַחֲסִי אחד את השני.
בנוסף, עקרון אי הוודאות מחייב כי תוצר אי הוודאות של שתי כמויות, כגון מיקום ומומנטום, תמיד יהיה גדול או שווה ל פלאנק קבוע (ח) חלקי 4π. עם זאת מקובל לראות את משוואת עקרון אי הוודאות שנכתבה במונחים של הקבוע של פלאנק מוּפחָת (? = h / 2π).
עקרון אי הוודאות של הייזנברג, המתייחס ל חוסר ודאותנותןעמדה של גוף עם חוסר הוודאות לגבי המומנטום שלה, מוגדר באמצעות המשוואה למטה:
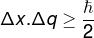
Δx - אי ודאות במיקום (מ ')
ש - חוסר וודאות של מומנטום (m / s)
? - קבוע פלאנק מופחת (1.0545.10−34 J.s)
עקרון אי הוודאות מוחל גם על האנרגיה וטווח הזמן של הגוף. שעון:

Δ ו חוסר ודאות באנרגיה (J)
t חוסר ודאות בזמן / ים
נניח, למשל, שבניסוי נתון אתה רוצה למדוד את עמדה של אלקטרון. על מנת להיות מסוגל למדוד את מיקומו, יש צורך כי איכשהו ייפלט פוטון לעבר האלקטרון הזה. עם זאת, כאשר פוטון משתקף בחזרה אל המתבונן, האלקטרון נרתע, מכיוון שהפוטון מעביר אליו כמות קטנה של תנועה ביחס ישר לו תדירות. אם אנו רוצים לקבוע בצורה מדויקת יותר את מיקומו של אלקטרון זה, אנו יכולים להגדיל את תדירות הפוטון. עם זאת, אם נעשה זאת, נגדיל את כמות התנועה הניתנת לאלקטרון, וכך נאבד את הדיוק במדידת גודל זה.
תראהגַם: מהי תורת המיתרים?
תרגיל נפתר על עקרון אי הוודאות
מדידת מעבדה מדויקת ביותר מסוגלת לקבוע את המיקום של מולקולה עם אי וודאות בסדר השווה ל- ± 10-15 M. על פי עקרון חוסר הוודאות, מהו האי-ודאות הקטנה ביותר האפשרית במדידת המומנטום של מולקולה זו?
פתרון הבעיה
עקרון אי הוודאות קובע כי תוצר אי הוודאות במיקום ובמומנטום חייב להיות גדול או שווה למחצית מקבוע הפלאנק המופחת:

לפיכך, לקיחת המודול של אי-הוודאות במיקום (Δx = 10-15) המסופק על ידי התרגיל ומודול הקבוע של פלאנק המופחת (? = 1,0545.10−34 J.s), נצטרך:

התוצאה שלעיל מציינת כי גם אם במעבדה יש מכשיר כלשהו המסוגל למדוד את כמות התנועה של חלקיק זה עם שגיאות קטנות מ- 10-20 M, לא ניתן יהיה למדוד את ערכו במדויק. לפיכך, תמיד יהיה לנו הערך המחושב לעיל כסטיית פלוס מינוס.
על ידי רפאל הלרברוק
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-principio-incerteza.htm
