במחקר התרמולוגיה אנו קוראים לזה טרנספורמציות אדיאבטיות אותן טרנספורמציות גזיות שבהן אין חילופי חום עם הסביבה החיצונית. לכן, בשינוי האדיאבטי החום הוא אפס.
ש = 0
אם אנו מיישמים את החוק הראשון של התרמודינמיקה, יש לנו:
Q = ∆U + τ
∆U = - τ
אבל מה הפירוש של חילופי חום בין הסביבה החיצונית? המשמעות היא שאם מתרחשת התפשטות גזית והגז מבצע עבודה של 300 J, זה לא קורה אם יש חילופי חום עם המדיום, הווריאציה של האנרגיה הפנימית של הגז תהיה שלילית, לכן תהיה לנו:
∆U = - 300 J
כעת, אם יש ירידה באנרגיה הפנימית של הגז, אנו יכולים לומר שהייתה גם ירידה בטמפרטורת הגז. מהחוק הכללי של גזים

אנו יכולים לומר שאם הנפח גדל וטמפרטורת הגז תפחת, בהכרח לחץ הגז יקטן גם הוא. באופן כללי, אנו יכולים לומר כי הדבר קורה עם דחיסה, מכיוון שאם יש דחיסה, האנרגיה הפנימית של הגז תגדל, כך גם הלחץ יגדל.
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
מפת חשיבה: טרנספורמציה אדיאבטית
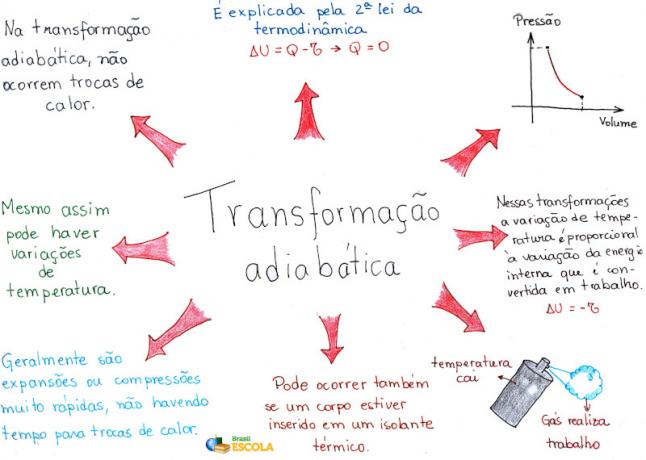
* להורדת מפת החשיבה ב- PDF, לחץ כאן!
בקצרה, אנו יכולים לומר כי:
- בהתרחבות adiabatic, הטמפרטורה והירידה בלחץ;
- בדחיסה אדיאבטית, גם הטמפרטורה וגם הלחץ עולים.
התרשים שלהלן נותן לנו סקירה על השינוי האדיאבטי:
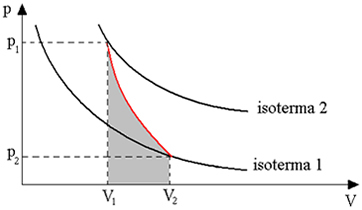
טרנספורמציות אדיאבטיות מתקבלות באמצעות מיכלים מבודדים תרמית, או גם באמצעות דחיסה או התרחבות מהירה מאוד.
לפיכך, אנו יכולים להסיק שכאשר גז מחליף חום עם הסביבה החיצונית, לוקח קצת זמן עד שהחום מתפשט דרך המסה הגזית והוא מגיע לשיווי משקל. לכן, כאשר מתרחשים גם הרחבה וגם דחיסה מהירה, אין כמעט חילופי חום עם הסביבה החיצונית.
* מפת חשיבה מאתי. רפאל הלרברוק
מאת דומיטיאנו מארקס
בוגר פיזיקה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
סילבה, דומיטיאנו קוראה מארקס דה. "חקר טרנספורמציה אדיאבטית"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/fisica/estudo-transformacao-adiabatica.htm. גישה אליו ב -27 ביוני 2021.