קורה ל טרנספורמציהאיזוכורי כאשר מסת גז נתונה עוברת שינויים ב טֶמפֶּרָטוּרָה שמפעילים שינויים בלחץ או להיפך, בהתחשב בטמפרטורה וב- לַחַץ, במקרה זה, הם כמויות מידתיות ישירות, בעוד נפח המערכת נותר ללא שינוי.
ראה גם: מהו לחץ חלקי של גזים?
מהו טרנספורמציה איזוכורית?
שינוי איזוכורי הוא כאשר שינוי בטמפרטורה ולחץ קורה למסת נתונה של גז, אך נפחו נשאר זהה. שינוי הלחץ יהיה ביחס ישר לטמפרטורהכלומר, אם גז, במערכת סגורה מסוימת, מכפיל את הטמפרטורה המוחלטת שלו, הדבר יגרום לעליית לחץ לכפליים ממה שהיה בתחילה.
סוג זה של טרנספורמציה נקרא גם איזובומומטרי או איזומטרי. המונח האיזוכורי מקורו ביוונית איזוכורה, על מה איזו פירושו "שווה" ו חורה פירושו "מקום או נפח" (בהקשר זה).
דוגמאות:
צמיגי המכונית עוברים טרנספורמציה איזוכורית, אנו יכולים לבחון זאת כאשר אנו מייצרים אותה כִּיוּל. בימים חמים הלחץ הניתן על צג הכיול גבוה יותר מאשר בימים קרים. הסיבה לכך היא שעם עליית הטמפרטורה הלחץ עולה מאחר והנפח נשאר.

דוגמאות נוספות הן ריסוס דאודורנטים, בסוג זה של מוצר יש אזהרה על התווית שלא לאחסן או לחשוף לטמפרטורות גבוהות, מכיוון שבנוסף לחלק מחומריו דליקים, קיים מצב של טרנספורמציה איזוכורית או איזובולומטרי. מכיוון ש דאודורנטים האירוסולים נמצאים בתוך בקבוק אטום ובמצב גזי,
טמפרטורה מוגברת תוביל להגברת הלחץ ולסיכון לפיצוץ.אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
מאפיינים של טרנספורמציה איזוכורית
- נפח קבוע.
- לחץ וטמפרטורה הם פרופורציונליים באופן ישיר.
ניתן לתאר מאפיינים אלה באמצעות הנוסחאות הבאות:

גרף של פונקציה איזוכורית
שימו לב לטבלה הבאה המתארת את התנהגות הגז ביחס ללחץ, לטמפרטורה ולקבוע המתקבל.
טמפרטורה (° C) |
לחץ (כספומט) |
P / T = קבוע |
50 |
5 |
10 |
100 |
10 |
10 |
150 |
15 |
10 |
200 |
20 |
10 |
שים לב שלחץ עוקב אחר עליית הטמפרטורה כך שיחס ה- P / T נשאר קבוע, כלומר הלחץ והטמפרטורה הם כמויות פרופורציונליות ישירות. לכן, הגרף המתאר טרנספורמציות איזוכוריות הוא מסוג ליניארי. תראה:

מי גילה את השינוי האיזוכורי?
ז'אק אלכסנדר סזאר צ'ארלס (1746-1823) היה המדען הצרפתי שבחן את התנהגות הגזים במערכת סגורה ליצירת מדחום מדויק, סיים את המחקרים על טרנספורמציות איזוכוריות.
המדען ג'וזף לואי גיי-לוסאק (1778-1850) פיתח גם מחקר על הרחבה והתכווצות של מערכת גזית. אלה היו ניתוחים עצמאיים, אך מכיוון שהגיעו לאותה מסקנה, הם חילקו את הזיכויים. כיום ישנם מחברים המתייחסים לשני החוקים הפיזיקליים האחרונים של גזים המסבירים את טרנספורמציות איזובריות ואיזוכורי כמו החוק הראשון והשני של צ'ארלס-גיי-לוסאק.
ראה גם: החוק הנפחי של גיי-לוסק
תרגיליםנפתרה
שאלה 1 - (PUC-RJ) צמיג אופניים מכויל בלחץ של 4 אטמוספרות, ביום קר, בטמפרטורה של 7 מעלות צלזיוס. נפח וכמות הגז המוזרק זהים. מה יהיה לחץ הכיול בצמיג כאשר הטמפרטורה תגיע ל 37 מעלות צלזיוס?
א) כספומט 21.1
ב) 4.4 כספומט
ג) 0.9 כספומט
ד) 760 מ"מ כספית
ה) 2.2 כספומט
פתרון הבעיה
חלופה א
שלב ראשון: זיהוי המערכת וחילוץ הנתונים.
מערכת איזובולומטרית
P1 = 4 כספומטים
T1 = 7 מעלות צלזיוס
T2 = 37 מעלות צלזיוס
P2 =?
באמצעות הנוסחה:
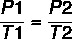
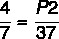
7 x P2 = 37 x 4
P2 = 148/7
P2 = 21.14 כספומט
שאלה 2 - (Unifor-CE) בחן את האיור שלהלן.
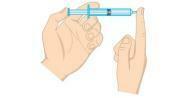
ניתן להפחית את לחץ הגז בתוך המזרק:
א) הנחת המזרק במי קרח, תוך שמירה על הקצה מכוסה.
ב) סחיטת הבוכנה, תוך שמירה על הקצה מכוסה.
ג) הנחת המזרק במים חמים, תוך שמירה על הקצה מכוסה.
ד) פתיחת הקצה והוצאת מחצית האוויר מתוך המזרק.
ה) משיכת הבוכנה, שמירת הקצה פתוח.
פתרון הבעיה
חלופה א '. הלחץ של גז הוא ביחס ישר לטמפרטורה במערכת איזוכורית, כלומר מבלי לשנות את נפח הגז או מסתו. כשיש ירידה בטמפרטורה, תהיה גם ירידה בלחץ.
מאת ליסה ברנרדס מארקס דה אראוג'ו
מורה לכימיה
האם תרצה להתייחס לטקסט זה בבית ספר או בעבודה אקדמית? תראה:
ARAúJO, ליסה ברנרדס מארקס דה. "טרנספורמציה איזוכורית (איזובומומטרית)"; בית ספר ברזיל. אפשר להשיג ב: https://brasilescola.uol.com.br/quimica/transformacao-isocorica.htm. גישה אליו ב -27 ביוני 2021.