ניתוק של בסיסים זה תהליך פיזי המתרחשת עם קבוצה חשובה זו של חומרים אנאורגניים כאשר הם מומסים במים, או כאשר הם עוברים את תהליך ההיתוך (מעבר ממצב מוצק למצב נוזלי דרך הַסָקָה).
באופן כללי, התופעה של דיסוציאציה בסיסית זה שחרור הקטיונים והאניונים שיוצרים את סריג יוני, שבמקרה זה הוא הבסיס. אז, במהלך דיסוציאציה בסיסית, שחרורו של יונים שכבר קיימים במתחם, כלומר לא נוצרים יונים חדשים.
הבסיס נוצר על ידי כל מתכת (X) שהיא הקטיון של התרכובת, או על ידי קטיון האמוניום (קבוצת NH4+), קשורה לאניון ההידרוקסיד (מיוצג על ידי קבוצת OH), כמו בייצוגים שלהלן:
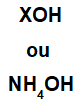
ייצוגים כלליים של נוסחת בסיס
בצורה מייצגים את דיסוציאציה בסיסית זה נעשה באמצעות משוואה שבה, במגיב יש לנו את הבסיס, ובמוצרים יש לנו את היונים (קטיונים ואניונים). מה שעושה את ההבדל הוא כיצד מתרחש הדיסוציאציה:
פירוק הבסיס במים:
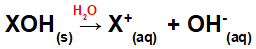
משוואה המייצגת את הניתוק של בסיס במדיום מימי
ניתוק לפי מיזוג בסיס:
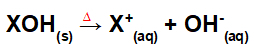
משוואה המייצגת את הניתוק של בסיס בתהליך ההיתוך
בניתוח המשוואות הכלליות לעיל, אנו מוודאים כי בכולן תמיד יהיה לנו הבסיס, הקטיון (שהוא קבוצת המתכת או NH4+) והאניון (OH-). אבל האם כולם כאלה? האם אין הבדל ביניהם? לשאלה הראשונה התשובה היא לא ולשאלה השנייה התשובה היא כן.
כאשר אנו מבצעים את ניתוק מבסיסראשית, יש לנתח את נוסחת הבסיס מכיוון שניתן לקבוע ממנה את העומס של קטיון וכמות המול של אניוני הידרוקסיד, מכיוון שכמות המול של הקטיון היא סטנדרטית (תמיד 1 מול).
כדאי לזכור שכמות קבוצות ה- OH הקיימות בנוסחת הבסיס קובעת את מטען הקטיון ואת הכמות במול של האניון ההידרוקסיד בדיסוציאציה של הבסיס.
בואו נסתכל על הדוגמאות של אלומיניום הידרוקסיד [Al (OH)3] והידרוקסיד זהב (AuOH). בנוסחת בסיס האלומיניום יש שלוש קבוצות OH, ובנוסחת בסיס הזהב רק קבוצת OH אחת. לפיכך, בדיסוציאציה של בסיסים אלה, יש לנו:
ניתוק אל (OH)3:
מכיוון שבסיס זה יש שלוש קבוצות OH בנוסחה, המטען על הקטיון יהיה +3 והכמות במול של אניונים שווה ל- 3 מול, כפי שניתן לראות במשוואה הבאה:
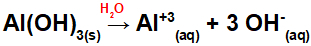
משוואת ניתוק בסיס אלומיניום במדיום מימי
ניתוק מ- AuOH:
מכיוון שבסיס זה יש קבוצת OH בנוסחה, המטען על הקטיון יהיה +1 והכמות במול של אניונים שווה ל- 1 מול, כפי שניתן לראות במשוואה הבאה:
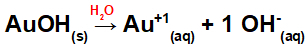
משוואת דיסוציאציה בסיסית לזהב במדיום מימי
על ידי. דיוגו לופס דיאס
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-dissociacao-das-bases.htm
