פתרון הוא תערובת הומוגנית של שני חומרים או יותר.. כמו, למשל, תמיסת מלח (מומס) מומסת במים (ממס).

במיוחד במעבדות כימיות ובתעשיות, תהליך זה חשוב מאוד מכיוון שהכימאי צריך להכין פתרונות בריכוזים ידועים. יתר על כן, בפעילויות ניסיוניות משתמשים בתמיסות עם ריכוזים נמוכים מאוד, כך שמדגם של הפתרון המרוכז מדולל לריכוז הרצוי.
על בסיס יומיומי, מספר פעמים, מבלי שאנו מבינים זאת כלל, אנו מבצעים את תהליך הדילול. לדוגמא, אריזות של מוצרי ניקוי והיגיינה ביתיים, כמו חומרי חיטוי, מייעצות לדלל אותן לפני השימוש. יש יצרנים שמציעים על תוויות המוצרים לדלל אותם במים בשיעור של 1 עד 3, כלומר לכל חלק במוצר יש להוסיף 3 חלקי מים. זה נעשה מכיוון שהמוצר מרוכז וחזק מאוד ועלול לפגוע במקום בו הוא מוחל אם הוא לא מדולל בצורה הנכונה. מצד שני, אם אתה מדלל אותו יותר ממה שהוא צריך, אתה יכול להפסיד כסף, כי המוצר לא ישיג את התוצאה הרצויה.

דוגמא נוספת היא כשאנחנו מכינים מיצים. על התוויות של תרכיזי מיץ רבים יש לדלל או לערבב כוס מיץ עם 5 כוסות מים. לפיכך, המיץ הופך ל"חלש "יותר, כלומר פחות מרוכז.
תאר לעצמך שדיללת מיץ כזה ב -3 ליטר מים. אם ריכוז המיץ הראשוני היה 40 גרם / ליטר, פירוש הדבר שהיה לו מסה של 40 גרם לכל ליטר ממס. אך מכיוון שיהיה לנו 3 ליטר, המסה תחולק ב -3 והריכוז יהיה אז בערך 13, 33 גרם / ליטר, או 13 גרם לכל ליטר תמיסה. עם זאת, בפתרון כולו, המסה של המומס 40 גרם עדיין נותרה.
חישוב הריכוז החדש הזה יכול להיעשות באופן הבא:
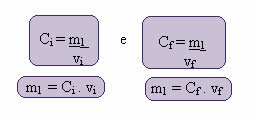
כאשר האינדקסים i ו- f מייצגים, בהתאמה, את הערכים הראשוניים והסופיים. מכיוון שערך m1 לא השתנה, אנו יכולים להשוות את המשוואות:
Çאני. vאני = גf. vf
החלפת הערכים שיש לנו, על פי הדוגמה הקודמת, שימו לב:
פיתרון ראשוני:
Çאני: 40 גרם / ליטר
m1: 40 גרם
vאני: 1 ליטר
פתרון סופי:
Çf: ?
m1: 40 גרם
vf: 3 ליטר
Çאני. vאני = גf. vf
(40 גרם / ליטר). (1 ליטר) = C.f. 3L
Çf = 40 גרם / ליטר
3
Çf = 13.333 גרם / ליטר
אותה נימוק תקף גם לריכוז הטוחנת (M) ולאחוז במסה של מומס או כייל (T):
Mאני. vאני = Mf. vf ו טאני. vאני = Tf. vf
מאת ג'ניפר פוגאצה
בוגר כימיה
צוות בית הספר בברזיל
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/diluicao-solucoes.htm

