דיפוזיה והתפשטות הם שני חוקים שהוצע על ידי הכימאי הסקוטי תומאס גרהאם, במאה ה -19, בהתבסס על מחקריו בנושא תערובות גז וההתנהגות של גזים כשעוברים בין קירות מכולה.
בין התצפיות שערך תומאס גרהם על התנהגות הגזים ביחס לדיפוזיה ואשפה, אנו יכולים להדגיש את הדברים הבאים:
לגז תמיד יש נטייה לעבור דרך חורים קטנים הקיימים בחומר מצב מוצק;
ככל שהגדול יותר מסת מולקולה גז, ככל שקושיו לעבור דרך חורי חומר מוצק;
ככל שצפיפות הגז נמוכה יותר, כך מהירות התנועה שלה גדולה יותר;
ככל שהטמפרטורה אליה נתון גז גבוהה יותר, כך המהירות בה הוא מתפשט לסביבה או עוברת דרך פתח גדולה יותר;
- גז לעולם לא נשאר סטטי במיקום מסוים.
ריכוך
ריכוך זו תופעה פיזיקלית המורכבת מיכולתו של גז להתפזר (כלומר להתפשט) בכל חלל האזור או בתוך מיכל. מסיבה זו, אנו יכולים לומר כי בתוך חלל, גז לעולם אינו מוגבל למיקום אחד.

ייצוג של התרחשות השידור
בנוסף, אנו יכולים להגדיר את ריכוך עדיין היות היכולת שיש לגז אחד לערבב עם אחר, כאשר הוא מונח באותה מיכל, ויוצר תערובת גזית הומוגנית.
דוגמא לכך היא כאשר גזים יוצאים מתפיחי הרכב. עד כמה שהם רעילים, הם אינם גורמים נזק לטווח קצר לבני אדם, מכיוון שהם מתפשטים באוויר האטמוספרי, וכתוצאה מכך מפחיתים את הריכוז שלהם.
הִשׁתַפְּכוּת
הִשׁתַפְּכוּת זו תופעה פיזיקלית המורכבת ממעבר גז דרך חורים הקיימים בדפנות מיכל מסוים, כלומר הוא מורכב ביציאה של גז מסביבה אחת לאחרת.

ייצוג של התרחשות השתפכות
דוגמה לכך היא כאשר הבלונים מנופחים למסיבה, ולמחרת, כולם מנופחים, הכל בגלל האוויר שנמלט דרך החורים הכלולים בבלונים.
חישובים הקשורים לדיפוזיה ותפליט
אנו יכולים לחשב, על פי משוואות שהציע גרהם, את המהירות שבה פועל גז דיפוזיה או התפשטות. לדברי גרהם, קצב התפוצה וההזרמה של שני גזים המעורבים במיכל הם תמיד ביחס הפוך לריבוע צפיפותם היחסית או המסה הטוחנת שלהם.
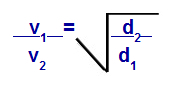
חוק גרהם ביחס לצפיפות
v1 = מהירות (התפשטות או דיפוזיה) של גז 1 בתערובת;
v2 = מהירות (התפשטות או דיפוזיה) של הגז 2 בתערובת;
ד1 = צפיפות הגז 1 של התערובת;
ד2 = צפיפות הגז 2 של התערובת;
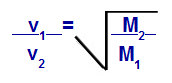
חוק גרהם הנוגע למיסה טוחנת
v1 = מהירות (התפשטות או דיפוזיה) של גז 1 בתערובת;
v2 = מהירות (התפשטות או דיפוזיה) של הגז 2 בתערובת;
M1 = מסת טוחנת של גז 1 של התערובת;
M2 = מסת טוחנת של גז 2 בתערובת.
על ידי. דיוגו לופס דיאס
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-difusao-efusao.htm
