בסיס הוא חומר אנאורגני אשר, על פי הכימאי השבדי סוואנטה ארחניוסכאשר הוא ממוקם במים, סובל מהתופעה של דיסוציאציה יונית, שבו יש את השחרור של יונים: קטיון (י+) ואניון הידרוקסיד (OH-).

נוסחה כללית של בסיס Arrhenius
קבוצת Y של א בסיס זה יכול להיות כל מתכת או אחרת מקבוצת האמוניום (NH4+), המשתחררים במים כקטיונים במהלך דיסוציאציה, כפי שניתן לראות במשוואה המייצגת את התהליך:
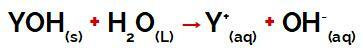
משוואה המייצגת את הניתוק של בסיס
ראה להלן מידע חשוב ביותר בנוגע לסיווג ולמינוח של בסיסים.
1) סיווג לגבי מסיסות של בסיסים(יכולת ל להתמוסס במים)
בסיסים מָסִיס: יש מתכת אלקלית או אמוניום בהרכב;
בסיסים מסיס במשורה: יש מתכת אדמת אלקליין בהרכב. דוגמה: מגנזיום הידרוקסיד, בשימוש נרחב כנוגד חומצה ומשלשל;
בסיסים באופן מעשי לֹא מָסִיס: יש מתכת אחרת בהרכב. דוגמה: הידרוקסיד מאלומיניום, בשימוש נרחב כנוגדי חומצה.
2) סיווג לגבי כוח שורש(יכולת ל להתנתק במים)
בסיסים חָזָק: יש מתכות אלקליות או אלקליין, למעט מגנזיום, בהרכב;
בסיסים חלש: יש מתכת אחרת בהרכב.
3) מינוח בסיס
כדי לקרוא שם לבסיס, פשוט עקוב אחר כלל השמות למטה:
הידרוקסיד + שם + מתכת או אמוניום
דוגמא: Ca (OH)2 → סידן הידרוקסיד
אם לבסיס יש יסוד כימי שאינו שייך למשפחות IA, IIA או IIIA (וזה לא ה- כסף או אבץ), עלינו לציין מול שם האלמנט, בספרות רומיות, את מספר הידרוקסילים:
דוגמא: Ti (OH)4 → טיטניום הידרוקסיד IV
על ידי. דיוגו לופס
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-base.htm

