בתרופות רבות ובמוצרי מזון נוזליים ומוצקים, כגון חומץ וביסקוויטים, למשל, תוכן באחוז המסה של המומס (מ '1) ביחס למסת התמיסה כולה (m = m1 + מ '2). גודל זה נקרא כותרת (T) או אחוז המוני של פיתרון.
ההגדרה שלה יכולה לבוא לידי ביטוי כדלקמן:

לפיכך, חישובו נעשה באמצעות המשוואה המתמטית להלן:
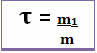
אוֹ

מכיוון שגם המכנה וגם המונה עוסקים באותה יחידה (יחידת המסה היא הגרם - גרם), לכותרת אין יחידה והיא קטנה מ -1.
לפיכך, אם אנו אומרים שכותרתו של פתרון נתון היא 0.4, המשמעות היא שלכל יחידת מסה של התמיסה, 0.4 תואם את מסת המומס. עם זאת, הכותרת מתבטאת לעיתים קרובות באחוזים. לשם כך, פשוט הכפל את הערך שנמצא ב 100%. במקרה זה זה נקרא אחוז המוני (ט%) *
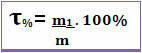
שימו לב לדמות שלהלן, בה ניתן אחוז המסה של נתרן כלורי בתמיסת מלח:

מלוחים, המשמשים לטיפול בהתייבשות, מכילים אחוז מסה של נתרן כלורי ב- 0.9%
במקרה זה, המשמעות היא שלכל 100 גרם או 100 יחידות של תמיסה זו יש 0.9 גרם או 0.9% של המומס, כלומר של נתרן כלורי (NaCl - מלח שולחן).
דוגמה נוספת היא חומץ: על התווית שלו יש אינדיקציה לכך ששימשו להכנתה 5% ממסת החומצה האצטית, כלומר יש 5 גרם של חומצה זו על כל 100 גרם תמיסה.

הכותרת יכולה להינתן גם ב אחוז נפח. במקרה זה, ההבדל היחיד הוא שבמקום להתייחס למסת המומס למסת התמיסה; נפח המומס קשור לנפח התמיסה, על פי הנוסחה הבאה:
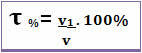
לדוגמא, במקרה של אלכוהול רגיל, שיש בו אחוז לפי נפח של 96%, ב 100 מ"ל של תמיסה, 96 מ"ל הוא אלכוהול.

* המונח "כותרת" משמש יותר בקרב מדענים, בעוד שטכנאים וכמה מחברי ספרים משתמשים בביטוי "אחוז המוני" לעתים קרובות יותר.
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/titulo-ou-porcentagem-massa.htm


