אתה גזים הם נוזלים אשר, בניגוד לנוזלים, תופסים את כל השטח הזמין של המיכל בו הם מוגבלים. המולקולות המרכיבות את הגזים חופשיים לנוע ולפעול ביניהם ובין קירות המכל.
או גז מושלם או אידיאלי זהו גז אידיאלי, בעל מאפיינים מסוימים ועומד בתנאי חוק הגז הכללי וה המשוואה של קלפיירון.
מאפיינים של גזים מושלמים
אין אינטראקציה כבידה בין מולקולות;
בְּ התנגשויות בין המולקולות יש אלסטי לחלוטיןכלומר יש שימור מוחלט של אנרגיה קינטית;
מולקולות מציגות תנועה לא מסודרת ו מהירויות התלויות ישירות בערך טמפרטורת הגז;
הנפח התקין של כל מולקולה אינו משמעותי לחלוטין בהשוואה לנפח הכולל של הגז.
משתני מצב
לַחַץ, טֶמפֶּרָטוּרָה ונפח הם כמויות פיזיקליות סקלריות המאפיינים גז. כמויות אלה נקראות משתני מצב והם שומרים על יחסים של מידתיות.
ה חוק בוילקובע שהקשר בין לחץ ונפח של גז הוא פרופורציונאלי הפוך. ככל שהלחץ על המולקולות גדול יותר, כך הם תופסים פחות מקום.
ה חוק גיי-לוסקקובע שהקשר בין הנפח לטמפרטורה של גז הוא פרופורציונלי ישירות. ככל שהטמפרטורה של גז גבוהה יותר, כך גדלה התסיסה של המולקולות, אשר נוטות להתרחק זו מזו, ולהגדיל את החלל שתופס אותן.
חוק צ'ארלס קובע שהקשר בין לחץ לטמפרטורה של גז הוא פרופורציונלי ישירות. ככל שהטמפרטורה של גז גבוהה יותר, כך התסיסה המולקולרית גדולה יותר. לפיכך, שכיחות ההתנגשויות בין המולקולות לדפנות המיכל עולה, והופכת את לחץ הגז לגדול יותר.
ה משוואת clapeyron הוא מסנתז את שלושת החוקים שהוצגו לעיל וקובע קשר יחיד בין משתני המצב.
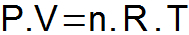
P = לחץ גז (כספומט או N / m2);
V = נפח גז (L או m3);
n = מספר שומות;
R = קבוע גז אוניברסלי (0.082 atm.l / mol. K או 8.31 J / mol. יא);
T = טמפרטורת הגז (K).
גז אידיאלי בטבע
הטבע אינו מייצר גזים בעלי מאפיינים של גז מושלם. הגז האידיאלי הוא מודל תיאורטי ושימושי להבנת התנהגות הגזים לנוכח שינויים במאפייניהם.
מאת ג'ואב סילאס
בוגר פיזיקה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/o-que-e/fisica/o-que-e-gas-perfeito.htm

