אחד תגובה הפיכה זה קורה כאשר ניתן להפוך את המוצרים חזרה למגיבים. תגובה מסוג זה נכנסת איזון כימי כאשר קצב התפתחות התגובה הישירה, כלומר התגובה עם צריכת ריאגנטים ויצירת מוצרים מתרחשים באותה מהירות כמו התגובה ההפוכה - יצירת מגיבים וצריכת מוצרים.
סוגים אלו של תגובות מאוזנות נראים הרבה בחיי היומיום. דוגמה היא מה שקורה במערות, ביצירת מה שנקרא נטיפים וזקיפים.
מי התהום נתונים ללחצים גבוהים ולכן הם מכילים כמויות גדולות של פחמן דו חמצני (CO2 (גרם)) מומס בו. כשעוברים בקרקעות המכילות אבן גיר (CaCO3 (ים)), פחמתי זה מתמוסס ומערות נוצרות, על פי התגובה למטה:
CaCO3 (ים) + CO2 (גרם) + H2או(1) → Ca2+(פה) + 2 HCO-3 (aq)
עם זאת, יונים של פחמתי וסידן יכולים להגיב ולהזרם מחדש כסידן פחמתי. זה מוכיח על ידי התגובה:
פה2+(פה) + 2 HCO-3 (aq)→ CaCO3 (ים) + CO2 (גרם) + H2או(1)
כפי ששמתם לב, תגובה אחת היא בדיוק ההפוכה מהאחרת: מגיבים הופכים למוצרים ומוצרים הופכים למגיבים. אז נוכל לייצג תגובה זו באיזון באופן הבא:
CaCO3 (ים) + CO2 (aq) + H2או(1) פה2+(פה) + 2 HCO-3 (aq)
פה2+(פה) + 2 HCO-3 (aq)
הרוח האיטית והרציפה של קרבונט מהטיפות המינרליזריות מגג המערות הולכות ונגלות, המים שלהן מתאדים ויש שחרור CO 2. אז האיזון הכימי מוסט בכיוון ההפוך (של יצירת ריאגנטים), ומכאן ה- CaCO3 (ים) נוצר, כלומר, ה נטיפים על גג המערות. בעת נפילה, הטיפה עדיין מומסה את הקרבונט, המופקד על רצפת המערה, ויוצר את סטלגמיטים.
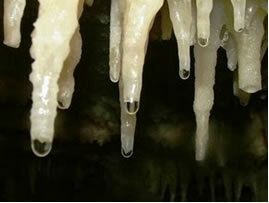
מים עם אבן גיר נוטפת ליצירת נטיפים וזקיפים
מאת ג'ניפר פוגאצה
בוגר כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/equilibrio-quimico-nas-cavernas.htm
