ה ריכוז נפוץ, הנקרא גם ריכוז ב-g/L, הוא היחס בין מסת המומס בנפח תמיסה.
מבחינה מתמטית, הריכוז הנפוץ בא לידי ביטוי באמצעות הנוסחה:
C = m/v
איפה,
C: ריכוז שכיח;
m: מסה של המומס;
V: נפח התמיסה.
היחידה הנפוצה ביותר לריכוז נפוץ היא g/L, שכן מסת המומס מחושבת בגרמים (g) ונפח התמיסה בליטר (L).
לדוגמה, במי ים יש כמות גדולה של מלחים מומסים ונתרן כלורי (NaCl), המכונה בפי העם מלח שולחן, הוא אחד מהם.
ריכוז הנתרן כלורי במי הים הוא, בממוצע, 2.5 גרם/ליטר. אז, יש 2.5 גרם של מלח, שהוא המומס, בכל 1 ליטר מי ים, שהוא הפתרון.
כיצד לחשב ריכוז נפוץ?
תמיסה היא תערובת הומוגנית שנוצרת על ידי חומר בכמות קטנה יותר, הנקרא מומס, מומס בממס, שהוא בכמות גדולה יותר.
לפיכך, ריכוז נפוץ מתייחס לכמות המומס בנפח נתון של תמיסה. ככל שמומסים יותר מומסים בתמיסה, כך היא מרוכזת יותר. אחרת, כלומר, מומס נמוך מצביע על כך שהתמיסה מדוללת.
דוגמה 1: מהו הריכוז ב-g/L של תמיסה של יודיד כסף (AgI) המכילה 2.6 גרם ב-1L של תמיסה?
כאשר נותנים את כמות המומס ונפח התמיסה, אנו פשוט מחברים את הערכים לנוסחת הריכוז הנפוצה כדי למצוא את ערכו.
לכן, בתמיסת 2.6 גרם/ליטר של יודיד כסף יש 2.6 גרם מומס בכל 1 ליטר תמיסה.
דוגמה 2: בעת אידוי הממס מ-500 מ"ל תמיסת מלח בריכוז של 6 גרם/ליטר, מהי מסת המומס המתקבלת?
שימו לב שבחישובים מסוימים, נוכל למצוא את הריכוז הנפוץ המתואר כך שנוכל לחשב את מסת המומס.
כמו כן יש לשים לב ליחידות. מכיוון שהריכוז הנפוץ ניתן ב-g/L, במקרה זה עלינו להמיר את יחידת הנפח לפני החלת הנוסחה.
כפי ש-1 ליטר מכיל 1000 מ"ל, כך 500 מ"ל מתאים ל-0.5 ליטר.
כך, בעת אידוי הממס מהתמיסה בריכוז של 6 גרם/ליטר, התקבלו 12 גרם מומס.
קבל יותר ידע עם התוכן:
- ריכוז תמיסה
- ריכוז מולארי
- דילול תמיסות
פתרו תרגילי ריכוז נפוצים
השתמש בשאלות הבאות כדי לבדוק את הידע שנרכש קודם לכן.
שאלה 1
(Unicamp) הממס מתאדה לחלוטין מ-250 מ"ל של תמיסה מימית של MgCl2 בריכוז 8.0 גרם/ליטר. כמה גרם של מומס מתקבלים?
א) 8.0
ב) 6.0
ג) 4.0
ד) 2.0
ה) 1.0
חלופה נכונה: ד) 2.0.
שאלה 2
ראה את התמונה למטה.
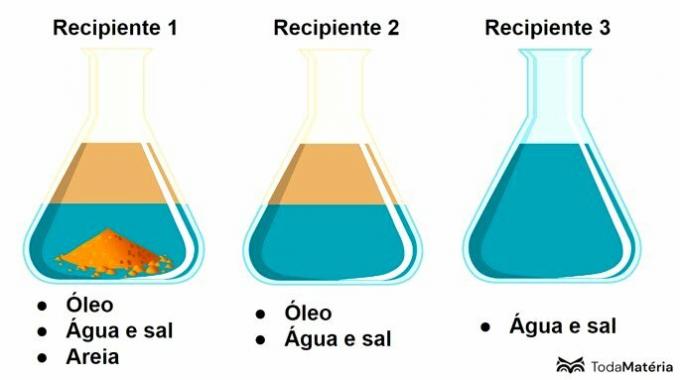
בתכנית זו, מיכל 3 מכיל א
א) תערובת הטרוגנית
ב) חומר טהור
ג) פתרון
ד) תערובת קולואידית
חלופה נכונה: ג) פתרון.
מיכל 3 מכיל תמיסה, שהיא תערובת הומוגנית שנוצרת על ידי מומס וממס, כאשר מלח הוא המומס ומים הם הממס.
באופן כללי, אנו יכולים לומר שהמומס הוא המרכיב בכמות הקטנה ביותר והממס קיים בכמות הגדולה ביותר.
מיכל 1 מציג תערובת הטרוגנית עם 3 פאזות ומיכל 2 מתאים לתערובת הטרוגנית של 2 פאזות.
שאלה 3
הוכנה תמיסה על ידי המסת 4.0 גרם מגנזיום כלוריד MgCl2 עד הגעה לריכוז של 2.0 גרם/ליטר. איזה נפח תמיסה הוכן?
א) 1 ליטר
ב) 2 ל'
ג) 4 ל'
ד) 6 ל'
חלופה נכונה: ב) 2 ליטר.
בדוק בעיות נוספות עם פתרון הערות בכתובת תרגילי ריכוז נפוצים.
הפניות ביבליוגרפיות
פונסקה, מ. ר. M. כימיה, 1. 1. ed. סאו פאולו: אטיקה, 2013.
SANTOS, W.L.P; MOL, G.S. כימיה אזרחית, 1. 2. ed. סאו פאולו: Editora AJS, 2013.
USBERCO, J. חבר כימיה, 1. 2. ed. סאו פאולו: סראיבה, 2014.
- תרגילים על ריכוז משותף עם משוב מוער
- פתרונות כימיים
- מומס וממס: מה הם, הבדלים ודוגמאות
- ריכוז תמיסה
- מְסִיסוּת
- מולריות או ריכוז מולארי: מה זה, נוסחה וכיצד לחשב
- דילול תמיסות
- תרגילים על תכונות החומר