נקרא דגם רתרפורד ההצעה שהציע המדען ארנסט רתרפורד לאטום ב-1911, במטרה להדגים את הצורה וההרכב האידיאליים של מרכיב החומר: אָטוֹם.
O דגם רתרפורד הוא מכונה בדרך כלל המודל של מערכת השמש, שכן המבנה ותפקודו הושוו ליחסים בין השמש לכוכבי הלכת שמסתובבים סביבה.
במודל שלו השווה רתרפורד את השמש לגרעין האטום, והאלקטרונים של האטום הושוו לכוכבי הלכת של מערכת השמש, כפי שניתן לראות בייצוג הבא:
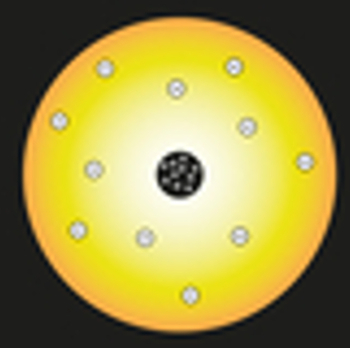
ייצוג המודל האטומי של רתרפורד
בתוך הגרעין ימוקמו חלקיקים בעלי מטען חיובי, הנקראים פרוטונים (שנתגלו על ידי יוגן גולדשטיין). הגרעין הזה יהיה קטן וצפוף ויהיה בעל המסה הגדולה ביותר של האטום.
הניסוי שביצע רתרפורד
כל ההצעות של רתרפורד ליצירת המודל האטומי שלו היו תוצאה של ניסוי שבו הוא מיקד אלומות קרינת אלפא (שמקורן של פולוניום רדיואקטיבי המצוי בקופסת עופרת) על לוח זהב דק, עם לוח מתכת מכוסה בגופרי אבץ מאחורי ובצדדים. הצדדים. אבץ גופרתי הוא מלח שכשהוא מקבל קרינה זורח.
רתרפורד ציין אז שלוש נקודות (a, b, c) זוהרו במיוחד במהלך הניסוי הזה:
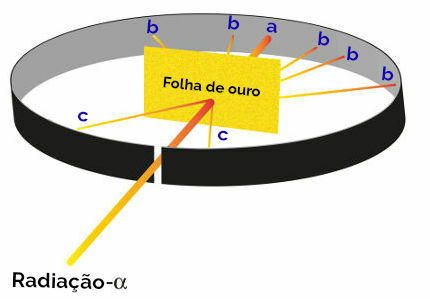
ייצוג ניסוי רתרפורד
-
נקודה א (שכיחות גבוהה יותר של ברק): ציינה שקרינת האלפא חצתה את לוח הזהב ללא כל בעיה, שכן היא תהיה בכיוון חור הפתיחה של גוש העופרת;
אל תפסיק עכשיו... יש עוד אחרי הפרסום ;)
נקודה ב (שכיחות קטנה של זוהר): ציינה שקרינת האלפא חצתה את לוח הזהב, אך היא הייתה סוטה במהלך החצייה;
נקודה ג (כמות קטנה ביותר של זוהר): ממוקם מול להב הזהב, הצביע על כך שקרינת אלפא לא עברה דרכה.
רתרפורד ייחס את התוצאות הנצפות הללו לאטומים היוצרים את לוח הזהב, תוך שהוא מפרש כדלקמן:
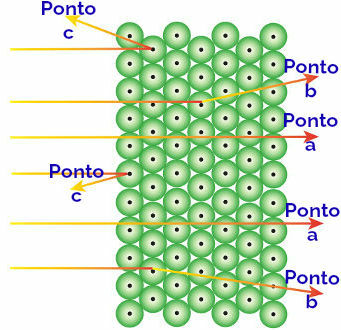
ייצוג התנהגות קרינת אלפא ואטומים
קרינת אלפא מגיעה ל מצביע על: קרינת אלפא היא חיובית ועוברת דרך אזור של האטום של חללים ריקים ענקיים. ישנם גם אלקטרונים בחלק מהאורביטלים.
קרינת אלפא מגיעה ל נקודה ב: קרינת האלפא עוברת דרך האטומים של לוח הזהב, אך היא מגיעה לרגע מסוים כאשר הוא עובר קרוב לגרעין הקטן של האטום, שהוא מטען חיובי, ויוצר דחייה ב קְרִינָה.
קרינת אלפא מגיעה ל נקודה ג: קרינת האלפא עוברת דרך האטומים של לוח הזהב, אך היא פוגעת בגרעין קטן, בעל מטען חיובי, ויוצר דחייה בקרינה.
בעייתיות של מודל רתרפורד
פיזיקאים רבים הצביעו על כמה בעיות במודל שהציע רתרפורד:
בעיה ראשונה: כיצד יתכן גרעין טעון חיובי אם חלקיקים בעלי מטען חיובי דוחים זה את זה?
בעיה 2: מדוע אלקטרונים באלקטרוספירות אינם נמשכים לפרוטונים בגרעין?
בעיה שלישית: מדוע אלקטרונים, שהם גופים קטנים בתנועה מתמדת, לא מאבדים אנרגיה ונופלים לתוך הגרעין?
*קרדיט תמונה: סוויק / Shutterstock
מאתי דיוגו לופס דיאס
האם תרצה להתייחס לטקסט זה בעבודה בית ספרית או אקדמית? תראה:
DAYS, דיוגו לופס. "מהו הדגם של רתרפורד?"; בית ספר ברזיל. זמין ב: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-modelo-rutherford.htm. נגיש ב-27 ביולי 2021.


