גם לאלדהידים וגם לקטונים יש קרבוניל כקבוצה פונקציונלית. ההבדל הוא במיקום הקרבוניל הזה. כפי שמוצג להלן, באלדהידים, הקרבוניל נראה קשור למימן, כלומר, הוא תמיד מגיע בסוף. מצד שני, בקטונים, קבוצת הקרבוניל נמצאת בין שני פחמנים, היא אף פעם לא מגיעה בסוף שרשראות הפחמן:
אלדהידים: קטונים:
OO
║║
ח Ç ─ ג ─ Ç ─C
השיטות העיקריות להשגת תרכובות השייכות לקבוצות אלו הן: הידרציה של אלקנים, אוזונוליזה של אלקנים וחמצון של אלכוהול. במקרה של קטונים, עדיין קיימת שיטה מיוחדת, והיא ה פירוק תרמי של מלחי סידן אורגניים.
ראה כיצד כל אחד מהתהליכים הללו פועל:
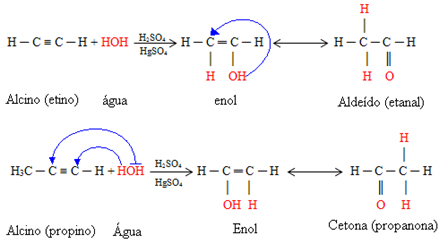
1. הידרציה אלקינים:הוספה של מולקולות מים מתבצעת בתווך חומצי בנוכחות זרז HgSO4.
בתחילה נוצרת תרכובת ביניים, אנול, אשר הופך לאלדהיד.
אם האלקין שמגיב הוא אתאן, תהיה לנו היווצרות האתנול האלדהיד. אבל אם זה כל אלקין אחר, הקטונים המתאימים יווצרו, בעקבות ה הכלל של מרקובניקוב, שבו המימן שבמים יוסיף לפחמן בקשר המשולש שהכי הרבה מימנים מחוברים אליו:
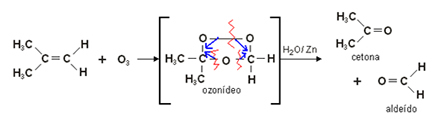
2. אוזונוליזה של אלקנים: אוזון (O3) מתווסף לקשר הכפול של האלקן, בתגובת חמצון בנוכחות מים ואבץ.
תחילה נוצרת תרכובת ביניים, אוזון, אשר עוברת הידרוליזה לאלדהיד ולקטון המקבילים.
להלן יש לנו את האוזונוליזה של 2-מתיל-פרופ-1-אן, היוצר פרופן-2-און ומתנול:
3. חמצון של אלכוהול: אלכוהול יכול לעבור חמצון כאשר הם נחשפים לחומר מחמצן, כגון תמיסה מימית של אשלגן דיכרומט (K2Cr2O7) או אשלגן פרמנגנט (KMnO4) במדיום חומצי.
אם אלכוהול הוא ראשוני, חמצון חלקי יוצר אלדהיד. אבל אם מדובר בחמצון מוחלט, האלדהיד יהפוך לחומצה קרבוקסילית. אם אנחנו רוצים לעצור באלדהיד, פשוט בצעו את התהליך הזה בטמפרטורה גבוהה מנקודת הרתיחה של האלדהיד שייווצר. בדרך זו, הוא מתאדה ומזוקק באמצעות מנגנון ספציפי.

אם האלכוהול הוא משני, תוצר החמצון שלו יהיה קטון.
דוגמא:
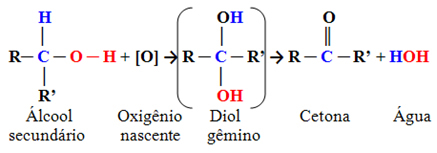
אלכוהול שלישוני אינו עובר חמצון.
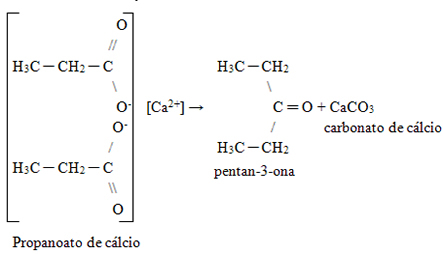
4. שיטה ספציפית להשגת קטונים: חימום מלחי סידן חומצה קרבוקסילית. מלחים אלו עוברים פירוק ומקורם, בנוסף לקטון, סידן פחמתי:
מאת ג'ניפר פוגאסה
בוגר לימודי כימיה
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/metodos-obtencao-aldeidos-cetonas.htm