הטבלה המחזורית היא כלי מחקר חשוב שאוסף מידע על כל היסודות הכימיים הידועים.
בדוק את הידע שלך באמצעות רשימה זו של 17 שאלות עם הגישות השונות בנושא ופתור את ספקותיך בעזרת ההחלטות שהוענקו לאחר המשוב.
כדי לעזור בהבנת השאלות, השתמש ב טבלה מחזורית מלא ומעודכן.
ארגון טבלה מחזורית
שאלה 1
(UFU) בתחילת המאה התשע עשרה, עם גילוי ובידוד של יסודות כימיים שונים, היה צורך לסווג אותם באופן רציונלי, על מנת לבצע מחקרים שיטתיים. תרומות רבות נוספו עד שהגיעו לסיווג התקופתי הנוכחי של יסודות כימיים. לגבי הסיווג התקופתי הנוכחי, תשובה:
א) כיצד מופיעים היסודות ברצף בטבלה המחזורית?
הטבלה המחזורית מאורגנת ברצפים של יסודות כימיים בסדר עולה מספר אטומי. מספר זה תואם את מספר הפרוטונים בגרעין האטום.
שיטת ארגון זו הוצעה על ידי הנרי מוזלי כאשר הוא הגדיר מחדש את הטבלה שהציע דמיטרי מנדלב.
אלמנט יכול להיות ממוקם בטבלה לפי המשפחה והתקופה בה הוא מוכנס. התפלגות זו מתרחשת באופן הבא:
| קבוצות או משפחות | 18 רצפים אנכיים |
| קבוצות של אלמנטים בעלי מאפיינים דומים. |
| תקופות | 7 רצפים אופקיים |
| מספר השכבות האלקטרוניות שיש לאלמנט. |
ב) אילו קבוצות בטבלה המחזורית ניתן למצוא: הלוגן, מתכת אלקלית, מתכת אדמת אלקליין, כלקוגן וגז אצילי?
סיווג האלמנטים לקבוצות נעשה על פי מאפיינים. לאלמנטים שנמצאים באותה קבוצה יש מאפיינים דומים ולסיווגים שניתנו עלינו:
| מִיוּן | קְבוּצָה | מִשׁפָּחָה | אלמנטים |
| הלוגן | 17 | 7 א | F, Cl, Br, I, At ו- Ts |
| מתכת אלקלית | 1 | 1 א | Li, Na, K, Rb, Cs ו- Fr |
| מתכת אדמת אלקליין | 2 | 2 א | Be, Mg, Ca, Sr, Ba and Ra |
| כלקוגן | 16 | 6 א | O, S, Se, Te, Po ו- Lv |
| גז אציל | 18 | 8 א | הוא, Ne, Ar, Kr, Xe, Rn ו- Og |
שאלה 2
(PUC-SP) פתר את הנושא על סמך ניתוח ההצהרות שלהלן.
I - הטבלה המחזורית המודרנית הנוכחית מסודרת בסדר עולה של המסה האטומית.
II - כל האלמנטים שיש להם אלקטרון אחד ו -2 אלקטרונים בקליפת הערכיות הם, בהתאמה, מתכות אלקליות ומתכות אדמה אלקליין, בתנאי שמספר הקוונטים העיקרי של שכבה זו (n 1).
III - באותה תקופה, האלמנטים מציגים את אותו מספר רמות (שכבות).
IV - באותה קבוצה (משפחה), לאלמנטים מספר זהה של רמות (שכבות).
המסקנה היא כי ביחס לטבלה המחזורית הנוכחית של יסודות כימיים הם נכונים:
א) IV ו- IV (בלבד).
ב) I ו- II (בלבד).
ג) II ו- III (בלבד).
ד) II ו- IV (בלבד).
ה) III ו- IV (בלבד).
חלופה נכונה: ג) II ו- III (בלבד).
ניתוח כל חלופה עלינו:
אני טועה. היסודות מסודרים בסדר עולה של מספר האטום.
II - נכון. האלקטרונים במעטפת הערכיות מגדירים את הקבוצה בה נמצא האלמנט.
| מתכות אלקליות | אלקטרון אחד במעטפת הערכיות |
| 3לקרוא | 2-1 |
| 11בְּ | 2-8-1 |
| 19ק | 2-8-8-1 |
| 37Rb | 2-8-18-8-1 |
| 55Cs | 2-8-18-18-8-1 |
| 87פר | 2-8-18-32-18-8-1 |
| מתכות אלקליות | 2 אלקטרונים במעטפת הערכיות |
| 4לִהיוֹת | 2-2 |
| 12מ"ג | 2-8-2 |
| 20פה | 2-8-8-2 |
| 38אדון | 2-8-18-8-2 |
| 56תוֹאַר רִאשׁוֹן | 2-8-18-18-8-2 |
| 88צְפַרְדֵעַ | 2-8-18-32-18-8-2 |
המספר הקוונטי הראשי תואם את הקליפה בה נמצא האלקטרון, כשהוא שונה מ- 1 בגלל על ידי ההפצה האלקטרונית אנו מבחינים כי מיקום האלקטרון הוא מהקליפה השנייה או n = 2.
III - נכון. מיקומו של אלמנט בתקופה מסוימת נובע ממספר השכבות בעת ביצוע ההפצה האלקטרונית.
| תקופות | 7 רצפים אופקיים |
| תקופה 1 | שכבה אחת: ק |
| תקופה 2 | 2 שכבות: K, L. |
| תקופה 3 | 3 שכבות: K, L, M |
| תקופה 4 | 4 שכבות: K, L, M, N. |
| תקופה 5 | 5 שכבות: K, L, M, N, O |
| תקופה 6 | 6 שכבות: K, L, M, N, O, P |
| תקופה 7 | 7 שכבות: K, L, M, N, O, P, Q |
דוגמא: יסוד כימי שנמצא בתקופה השנייה.
IV - שגוי. לאלמנטים השייכים לאותה קבוצה מאפיינים דומים וזה נובע מהעובדה שיש להם מספר זהה של אלקטרונים במעטפת הערכיות.
דוגמא:
| בריליום | מגנזיום |
|
2 אלקטרונים ב שכבת הערכיות. |
2 אלקטרונים ב שכבת הערכיות. |
לכן, בריליום ומגנזיום הם חלק מקבוצה 2 בטבלה המחזורית.
שאלה 3
(Unitins) לגבי הסיווג התקופתי המודרני של אלמנטים, זהה את האמירה האמיתית:
א) במשפחה, לאלמנטים יש בדרך כלל מספר זהה של אלקטרונים בקליפה האחרונה.
ב) בטבלה המחזורית, היסודות הכימיים ממוקמים בסדר יורד של מסות האטום.
ג) במשפחה, לאלמנטים יש תכונות כימיות שונות מאוד.
ד) בתקופה אחת, לאלמנטים יש תכונות כימיות דומות.
ה) כל האלמנטים המייצגים שייכים לקבוצה B של הטבלה המחזורית.
חלופה נכונה: א) במשפחה, לאלמנטים יש בדרך כלל מספר זהה של אלקטרונים בקליפה האחרונה.
א) נכון. לאלמנטים כימיים של אותה משפחה יש מספר זהה של אלקטרונים בקליפה האחרונה וזה גורם להם להיות מאפיינים דומים.
ב) לא נכון. מסות אטומיות גדלות ככל שמספר האטום של היסוד גדל.
ג) לא נכון. התכונות הכימיות של היסודות דומות, ולכן הן מקובצות באותה משפחה.
ד) שגוי. בעת ובעונה אחת, האלמנטים מחולקים באותם מספר קליפות.
ה) לא נכון. האלמנטים המייצגים שייכים לקבוצה A, המתאימה למשפחות: 1A, 2A, 3A, 4A, 5A, 6A, 7A ו- 8A. אלמנטים השייכים לקבוצה B הם אלמנטים מעבר.
שאלה 4
(Vunesp) בהתחשב בתכונות של יסודות כימיים ובטבלה המחזורית, לא נכון לציין:
א) מתכת הינה חומר המוליך זרם חשמלי, נמתח ונחלש.
ב) חומר שאינו מתכת הוא חומר שאינו מוליך זרם חשמלי, אינו נמשך ולא ניתן לגמישות.
ג) לחצי-מתכת מראה פיזי של מתכת, אך התנהגות כימית דומה לזו של מתכת.
ד) מרבית היסודות הכימיים מורכבים ממתכות.
ה) הגזים האצילים הם חד-אטומיים.
חלופה שגויה: ד) רוב היסודות הכימיים אינם מתכות.
שים לב לסיווג היסודות הכימיים בטבלה המחזורית למתכות, לא מתכות וחצי מתכת.

כפי שאנו רואים, רוב היסודות הם מתכות.
א) נכון. מתכות מוליכות חשמל בגלל ענני אלקטרונים הנוצרים על ידי אלקטרונים חופשיים, האופייניים למבנהם. הם רקיעיים בגלל שהם יכולים להפוך לחוטים או סדינים, בהתאם לאזור בו מופעל הלחץ. הם גם ניתנים לגמישה, מכיוון שניתן לייצר יריעות דקות מאוד עם חומר מסוג זה.
ב) נכון. לא מתכות יש מאפיינים הפוכים של מתכות. במקום מוליכים, הם מבודדים תרמיים טובים, ומכיוון שהם שבירים, הם לא מעוצבים לחוטים או יריעות מכיוון שאין להם משיכות וגמישות טובים.
ג) נכון. לחצי מתכות מאפיינים בינוניים למתכות ולא למתכות. בהיותם מוליכים למחצה של חשמל, יש להם ברק מתכתי אך הם שבירים כמו שאינם מתכות.
ד) שגוי. רוב היסודות מסווגים כמתכות. שיעורי המתכות הקיימים בטבלה המחזורית הם: אלקליין, אדמה בסיסית, פנימית וחיצונית מעבר.
ה) נכון. גזים אצילים הם חד-אטומיים, ולכן הם מיוצגים רק בראשי התיבות שלהם.
דוגמא:
| גז אציל | כלקוגן |
| הליום (הוא) | חמצן (O2) |
| מונואטומי: נוצר על ידי אטום | דיאטומי: נוצר על ידי שני אטומים |
בשל יציבותם של הגזים האצילים, לאלמנטים ממשפחה זו תגובתיות נמוכה והם ידועים גם כאי-אינרטיים.
שאלה 5
על ארגון הטבלה המחזורית הנוכחית, תשובה:
א) מהן עמודות?
ב) מהם הקווים?
ג) מהי השיטה בה משתמשים לארגון היסודות הכימיים?
תשובות:
א) העמודות הן קבוצות הטבלה המחזורית, שנקראה בעבר משפחות, המפגישות יסודות כימיים בעלי תכונות דומות.
ב) הקווים הם תקופות הטבלה המחזורית ומציינים את מספר השכבות האלקטרוניות של אטום במצב הקרקע.
ג) היסודות הכימיים בטבלה המחזורית הנוכחית מסודרים בסדר עולה של מספר האטום, המציין את מספר הפרוטונים בגרעין האטום.
משפחות טבלה מחזורית
שאלה 1
(CESGRANRIO) יצירת הקשר בין העמודות למטה, המתאימות למשפחות האלמנטים על פי הטבלה המחזורית, הרצף המספרי יהיה:
| 1. גזים אצילים | • קבוצה 1 א |
| 2. מתכות אלקליות | • קבוצה 2 א |
| 3. מתכות אלקליות | • קבוצה 6 א |
| 4. כלקוגנים | • קבוצה 7 א |
| 5. הלוגנים | • קבוצה 0 |
א) 1, 2, 3, 4, 5.
ב) 2, 3, 4, 5, 1.
ג) 3, 2, 5, 4, 1.
ד) 3, 2, 4, 5, 1.
ה) 5, 2, 4, 3, 1.
חלופה נכונה: ב) 2, 3, 4, 5, 1.
| קבוצות | תצורה אלקטרונית |
| • קבוצה 1 א: 2. מתכות אלקליות | לָנוּ1 (עם נ |
| • קבוצה 2 א: 3. מתכות אלקליות | לָנוּ2 (עם נ |
| • קבוצה 6 א: 4. כלקוגנים | לָנוּ2np4 |
| • קבוצה 7 א: 5. הלוגנים | לָנוּ2np5 |
| • קבוצה 0: 1. גזים אצילים | 1s2 (הוא) או אנחנו2np6 (אם n> 1) |
שאלה 2
(UECE) היסוד הכימי עם Z = 54 כולל בשכבת הערכיות את תצורת ה 5s2 5p6. האלמנטים עם Z = 52 ועם Z = 56 שייכים למשפחות של:
א) קלקוגנים ואדמה אלקליין
ב) הלוגנים ואלקליות
ג) הלוגנים ואדמה בסיסית
ד) כלקוגנים ואלקליות
חלופה נכונה: א) קלקוגנים וארצות אלקליין.
בהתחשב במספרים האטומיים, ביצענו את ההפצה האלקטרונית ומצאנו את התוצאות הבאות:
| 54X ו- | 52אתה | 56תוֹאַר רִאשׁוֹן |
|
8 אלקטרונים ב שכבת הערכיות |
6 אלקטרונים ב שכבת הערכיות |
2 אלקטרונים ב שכבת הערכיות |
| גזים אצילים: משפחה 8A | כלקוגנים: משפחה 6A | כדור הארץ אלקליין: משפחה 2 א |
שאלה 3
(פ. Ibero-Americana-SP) קבוצת הטבלה המחזורית המאופיינת בשליטה של יסודות מלאכותיים היא הבאה:
א) לנתנידים
ב) גזים אצילים
ג) מתכות מעבר
ד) מתכות אדמה אלקליין
ה) אקטינידים
חלופה נכונה: ה) אקטינידים.
יסודות מלאכותיים הם אלה שאינם קיימים בטבע ואשר סונתזו במעבדה באמצעות תגובות גרעיניות.
הם נקראים גם יסודות טרנסורניים, מכיוון שליסודות רדיואקטיביים אלה מספר אטומי גדול מ- 92, המקביל לאורניום.
באופן כללי, אלמנטים אלה הם קצרי מועד ונמשכים עד שברירי שנייה.
על פי מידע זה עלינו:
היסודות המצויים בטבע הם: לנתנידים, גזים אצילים, מתכות מעבר ומתכות אדמה אלקליין. למעט טכניציום ופרומתיום שהם מלאכותיים.
הדומיננטיות של יסודות מלאכותיים היא אקטינידים, המסווגים כמתכות מעבר פנימיות והוכנסו לטבלה המחזורית מתחת לנטנידים. מאותה סדרה רק אקטיניום, תוריום, פרוטאקטיניום ואורניום הם טבעיים.
שאלה 4
(U. הכנסייה הקתולית של סלבדור- BA) מינים X2- עם 8 אלקטרונים בקליפה החיצונית ביותר (מעטפת הערכיות) זה יכול להיות מרכיב X, אשר, בטבלה המחזורית, שייך לקבוצה:
א) 7 א
ב) 6 א
ג) 2 א
ד) 1 א
ה) 8 א
חלופה נכונה: ב) 6 א.
על פי כלל האוקטט, כדי שאלמנט יקנה יציבות, הוא מניח את התצורה האלקטרונית של גז אצילי, שיש לו 8 אלקטרונים במעטפת הערכיות.
תשלום 2- על מינים X2- מציין שהאלמנט צבר 2 אלקטרונים.
תצורת האלקטרונים של המינים בעלי 8 אלקטרונים בקליפה החיצונית ביותר היא ns2np6.
לאחר איבוד שני אלקטרונים, האלמנט חוזר למצבו הקרקעי עם תצורת אלקטרונים ns2np4.
6 האלקטרונים במעטפת הערכיות אופייניים לכלקוגנים, אלמנטים ממשפחת 6A.
לדוגמה:
| אלמנט: חמצן | תצורה אלקטרונית |
| 8או | 1s22s22p4 |
| מינים O2- | 1s22s22p6 |
למידע נוסף על משפחות טבלה מחזורית.
יסודות כימיים
שאלה 1
(CESGRANRIO) בהתחשב באלמנטים של המספרים האטומיים 3, 9, 11, 12, 20, 37, 38, 47, 55, 56 ו- 75, האפשרות שמכילה מתכות אלקליות בלבד היא:
א) 3, 11, 37 ו -55
ב) 3, 9, 37 ו -55
ג) 9, 11, 38 ו -55
ד) 12, 20, 38 ו -56
ה) 12, 37, 47 ו -75
חלופה נכונה: א) 3, 11, 37 ו -55
מתכות אלקליות תואמות את היסודות הכימיים המסיימים את ההתפלגות האלקטרונית עם אלקטרון ברמת המשנה.
בהפצה האלקטרונית של המספרים האטומיים הנתונים, יש לנו את המתכות האלקליות הבאות:
| Z = 3 | Z = 11 | Z = 37 | Z = 55 |
| לִיתִיוּם | נתרן | רובידיום | צזיום |
המספרים האטומיים האחרים תואמים לאלמנטים מהקבוצות הבאות:
מתכות אדמה אלקליין: מסיימות הפצה אלקטרונית ברמה תת2.
| Z = 12 | Z = 38 | Z = 56 |
| מגנזיום | סטרונציום | בריום |
מתכות מעבר: מסיימות הפצה אלקטרונית ברמת משנה d.
| Z = 30 | Z = 47 | Z = 75 |
| אָבָץ | כסף | רניום |
הלוגנים: הפסקת הפצה אלקטרונית ברמת משנה עמ '5.
| Z = 9 |
שאלה 2
(Unirio) "הלב המלאכותי שהונח באלואי החל להתפתח לפני ארבע שנים בארצות הברית וכבר משמש אותו כ -500 איש. הסט, הנקרא Heartmate, מורכב משלוש חלקים עיקריים. החשוב ביותר הוא תיק עגול של ארבעה קילו, שקוטרו 12 ס"מ ועובי 3 ס"מ, עשוי טיטניום - מתכת לבנה כסופה, קלה וחזקה. " מגזין Veja, יולי 1999.
בין המתכות למטה, זו שיש בשכבה האחרונה מספר אלקטרונים השווים לזה של טיטניום היא:
א) ג
ב) ב
ג) גא
ד) מג
ה) Xe
חלופה נכונה: ד) מג.
| טִיטָן | תצורה אלקטרונית | חלוקת שכבות |
| 22אתה | 1s2 2s2 2p6 3s2 3p6 4s2 3d2 | 2, 8, 10, 2 |
מההפצה האלקטרונית של טיטניום אנו רואים כי לאלמנט זה יש שני אלקטרונים בקליפה האחרונה.
| אֵלֵמֶנט | תצורה אלקטרונית | חלוקת שכבות |
| 6Ç | 1s2 2s2 2p2 | 2, 4 |
| 11בְּ | 1s2 2s2 2p6 3s1 | 2, 8, 1 |
| 31גא | 1s2 2s2 2p6 3s2 3p6 4s2 3d104p1 | 2, 8, 18, 3 |
| 12מ"ג | 1s2 2s2 2p6 3s2 | 2, 8, 2 |
| 54X ו- | 1s2 2s2 2p6 3s2 3p6 3d10 4s2 4p6 4d10 5s2 5p6 | 2, 8, 18, 18, 8 |
האלמנט שיש בו גם 2 אלקטרונים בקליפה האחרונה הוא מגנזיום.
שאלה 3
(UFPA) שקול יסוד כימי מסוים שרמת המשנה האנרגטית ביותר שלו היא 5s2. מספרו האטומי והקבוצה בה הוא נמצא על הטבלה המחזורית הם, בהתאמה:
א) 20; 1 א
ב) 20; 2 א
ג) 38; 2 א
ד) 38; 1 א
ה) 39; 2 א
חלופה נכונה: ג) 38; 2 א
על ידי ביצוע ההפצה האלקטרונית גילינו כי:
- היסוד הכימי ממוקם במשפחה 2 א, מכיוון שיש לו את רמת המשנה האנרגטית ביותר2
- בעל מספר אטומי 38המתאים למספר הכולל של האלקטרונים שהופצו.
- הוא ממוקם בתקופה החמישית, מכיוון שההפצה האלקטרונית בוצעה עד השכבה החמישית.
בבדיקת מידע זה בטבלה המחזורית נוכל לאשר שמדובר ביסוד סטרונציום.
שאלה 4
(UFC) לאטום x יש פרוטון אחד יותר מאטום y. על סמך מידע זה, קבע את ההצהרה הנכונה.
א) אם y הוא אדמה אלקליין, x הוא מתכת אלקלית.
ב) אם y הוא גז אצילי, x הוא הלוגן.
ג) אם y הוא מתכת מעבר, x הוא גז אצילי.
ד) אם y הוא גז אצילי, x הוא מתכת אלקלית.
ה) x ממוקם באותה תקופה לפני אטום y בטבלה המחזורית.
חלופה נכונה: ד) אם y הוא גז אצילי, x הוא מתכת אלקלית.
הטבלה המחזורית מסודרת לפי סדר עולה של המספר האטומי.
אם ל- Y יש מספר אטומי z ל- X יש פרוטון אחד יותר ממנו, המשמעות היא ששני היסודות הללו נמצאים באותה תקופה ו- X הוא לאחר מכן ל- Y.
דוגמא:
| אֵלֵמֶנט | אלמנט שלאחר מכן |
| zי | z + 1איקס |
| 11בְּ | 12מ"ג |
שני היסודות נמצאים בתקופה השלישית ולמגנזיום יש פרוטון אחד יותר מאשר נתרן.
על פי הנמקה זו עלינו:
שגוי. מתכת אלקלית באה לפני מתכת אדמה אלקליין בטבלה המחזורית. המשפט הנכון יהיה: אם y הוא מתכת אלקלית, x הוא אדמה אלקליין.
ב) לא נכון. הלוגן מגיע לפני הגז האצילי בטבלה המחזורית. המשפט הנכון יהיה: אם y הוא הלוגן, x הוא גז אצילי.
ג) לא נכון. מתכות מעבר וגזים אצילים מופרדים על ידי אלמנטים כימיים אחרים ולכן אינם רציפים.
ד) נכון. גזים אצילים הם הקבוצה האחרונה בטבלה המחזורית ומתכות אלקליות הראשונה, ולכן הן רציפות.
דוגמא:
| גז אציל | מתכת אלקלית |
| zי | z + 1איקס |
| 2הוא | 3לקרוא |
לליתיום, מתכת אלקלית, יש פרוטון אחד יותר מהליום, שהוא גז אצילי.
ה) לא נכון. X נמצא באותה תקופה כמו Y אך אחריה, לא מוקדם יותר כמו שהחלופות קובעות.
שאלה 5
מהמספר האטומי של יסוד כימי ניתן לדעת:
א) מספר הנויטרונים בגרעין
ב) מספר האלקטרונים באלקטרוספרה
ג) מסת הליבה
תשובה: ב) מספר האלקטרונים באלקטרוספרה
אטום במצב הקרקע הוא ניטרלי מבחינה חשמלית. לכן, בידיעת המספר האטומי, המתאים למספר הפרוטונים (חלקיקים טעונים חיובית), אנו יודעים את מספר האלקטרונים (חלקיקים טעונים שלילית) באלקטרוספרה.
לדוגמא, לברזל יש מספר אטומי 26, ולכן במצב הקרקע יש לו 26 אלקטרונים סביב הגרעין.
למידע נוסף על יסודות כימיים זה ה מספר אטומי.
תכונות תקופתיות ואפרודיאליות
שאלה 1
(UFSM) שפט אם ההצהרות הקשורות לתכונות התקופתיות של האלמנטים נכונות (T) או כוזבות (F).
() תלוי במסה האטומית של היסודות.
() הם חוזרים על עצמם במרווחי זמן קבועים פחות או יותר ביחס לעלייה במספרים האטומיים.
() דומים באותה קבוצת אלמנטים.
() דומים באותה תקופת אלמנטים.
() באותה קבוצה, הערכים המספריים של המאפיינים התקופתיים עולים תמיד כאשר יש עלייה במספר האטומים של היסודות.
הרצף הנכון הוא:
א) V - F - V - F - F
ב) V - F - F - V - V
ג) F - V - V - F - F
ד) F - V - F - V - V
ה) V - F - F - V - F
חלופה נכונה: ג) F - V - V - F - F
(שֶׁקֶרתלוי במסות האטומיות של היסודות.
על פי חוק המחזוריות של מוסלי, תכונות פיזיקליות וכימיות רבות של יסודות כימיים משתנות לפי המספר האטומי.
(נָכוֹן) הם חוזרים על עצמם במרווחי זמן קבועים פחות או יותר ביחס לעלייה במספרים האטומיים.
מאפיינים כמו רדיוס אטומי, נפח אטומי, צפיפות, נקודת התכה ורתיחה הם דוגמאות לתכונות החוזרות על עצמן בטבלה המחזורית.
(נָכוֹן) דומים באותה קבוצת אלמנטים.
קבוצות הטבלה המחזורית סודרו עם אלמנטים בעלי תכונות דומות.
(שֶׁקֶר) דומים באותה תקופת אלמנטים.
הנכסים דומים במשפחות, ולא בתקופות. בתקופות, האלמנטים מחולקים לפי מספר השכבות האלקטרוניות.
(שֶׁקֶר) באותה קבוצה, הערכים המספריים של המאפיינים התקופתיים עולים תמיד כאשר יש עלייה במספר האטומים של היסודות.
מאפיינים יכולים להגדיל או להקטין בהתאם למספר האטומי. דוגמה לכך היא אלקטרונטיביטיביות, אשר פוחתת ככל שמספר האטום גדל בקבוצה נתונה.
קרא גם: מאפיינים תקופתיים
שאלה 2
(FAESP) התכונות האפרודיאליות של היסודות הן:
א) צפיפות, נפח אטומי ומסה אטומית.
נקודת התכה, אלקטרונטיביות וחום ספציפי.
ג) נפח אטומי, מסת אטום ונקודת התכה.
ד) מסה אטומית, חום ונקודת התכה ספציפיים.
ה) מסה אטומית וחום ספציפי.
חלופה נכונה: ה) מסת אטום וחום ספציפי.
התכונות האפריודיאליות חוזרות על עצמן במרווחי זמן קבועים.
מסה אטומית היא המדד של משקל האטום ביחידות מסה אטומית, המתאים ל ממסת הפחמן 12.
חום ספציפי קובע את כמות החום הדרושה להגדלת הטמפרטורה ב -1 מעלות צלזיוס של 1 גרם של היסוד.
שני מאפיינים אלה אינם קשורים למיקום האלמנט בטבלה המחזורית.
המאפיינים האחרים מסווגים כתקופתיים ככל שהם גדלים או יורדים עם המספר האטומי. האם הם:
- צפיפות: מייצג את המרכיב בין המסה לנפח של אלמנט.
- נפח אטומי: מייצג את הנפח של קבוצת אטומים ומשפיע על המרחק ביניהם.
- נקודת התכה: טמפרטורה בה מתרחש המעבר בין מוצק לנוזל.
- אלקטרונטיביטיביות: יכולתו של האטום למשוך לעצמו את הזוג האלקטרוני שהוא חולק בקשר קוולנטי.
קרא גם: שליליות אלקטרונית ו זיקה אלקטרונית
שאלה 3
(PUC-PR) בין הדיאגרמות הבאות הקשורות לטבלה המחזורית, אילו מהן נכונות?
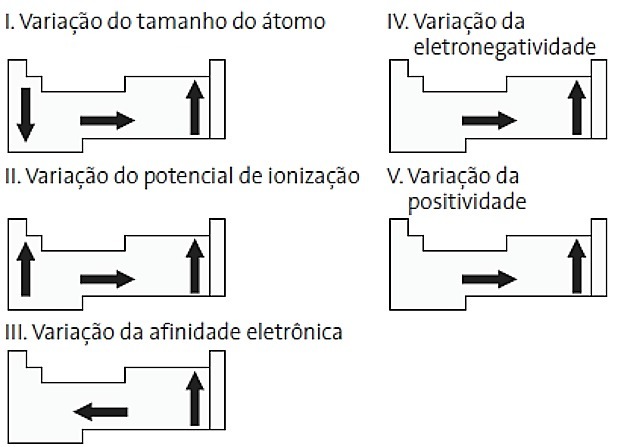
א) II ו- V.
ב) II ו- III
ג) אני ו- V.
ד) II ו- IV
ה) III ו- IV
חלופה נכונה: ד) II ו- IV.
אני. שגוי. וריאציה בגודל האטום נמדדת לפי המרחק הממוצע מהגרעין לאלקטרון החיצוני ביותר. האטומים הגדולים ביותר נמצאים בתחתית הטבלה, ולכן הגידול מתרחש בהתאם למספר האטומי והייצוג הנכון הוא:
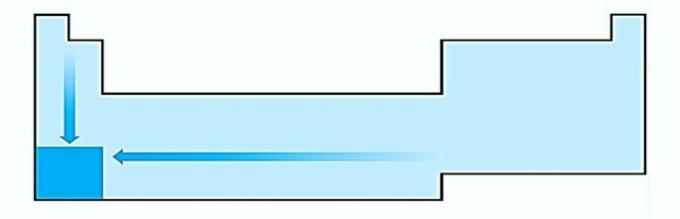
II. נכון האנרגיה הדרושה לקריעת אלקטרון מאטום מבודד במצב הגזי נקראת פוטנציאל יינון. זה גדל כפי שמוצג בתרשים ההצהרה.
III. שגוי. זיקה אלקטרונית מבטאת את האנרגיה המשתחררת כאשר אטום ניטרלי במצב הגזי מקבל אלקטרון, שהוא מאפיין חשוב מאוד של שאינם מתכות. הזיקות האלקטרוניות הגבוהות ביותר נצפות בהלוגנים ובחמצן.
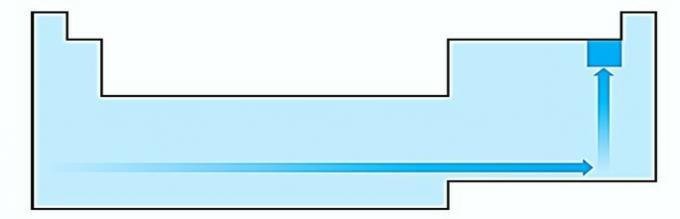
IV. נכון השלכות אלקטרוניות קשורות לפוטנציאל יינון ולזיקה אלקטרונית. ככאלה, הלוגנים הם האלמנטים האלקטרוניים ביותר בטבלה המחזורית.
V. שגוי. אלקטרופוזיטיביות מתרחשת בכיוון ההפוך לאלקטרואנגטיביות. הוא מייצג את יכולתו של האטום לוותר על אלקטרונים.
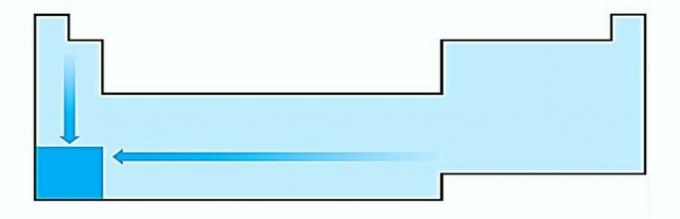
לכן, מתכות אלקליות הן בעלות החשמל הגבוה ביותר.
המשך לבדוק את הידע שלך ברשימות:
- תרגילים על קשרים כימיים
- תרגילים בנושא הפצה אלקטרונית
- תרגילים על מודלים אטומיים
- תרגילים בנושא תרמו-כימיה


