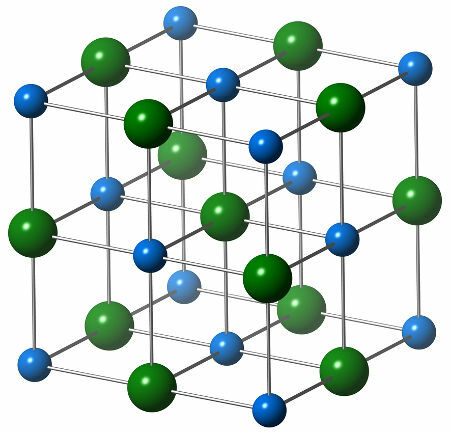
אטומים הם חלקיקים קטנים לאין ערוך המרכיבים את כל החומר ביקום. עם הזמן, הרעיון כיצד יהיה מבנה האטום השתנה בהתאם לתגליות חדשות שגילו מדענים. תוכלו לברר מידע נוסף על כך בטקסטהאבולוציה של המודל האטומי.
מודל הוא ייצוג של המציאות (לא המציאות עצמה), ולכן מודלים אטומיים הם ייצוגים של המרכיבים העיקריים של האטום ומבנהו ומסבירים התנהגות פיזיקלית וכימית מסוימת של חומר. זה נעשה מכיוון שעדיין אין אפשרות לאדם לראות אטום מבודד אפילו עם אולטרה מיקרוסקופים.
כדי לקבל מושג עד כמה האטום קטן, דע זאת ה החלקיק הקטן ביותר הנראה במיקרוסקופ רגיל מכיל למעלה מעשרה מיליארד אטומים! האטום כל כך קטן שאם היינו מניחים מיליון מהם זה לצד זה, לא היינו מגיעים ל עובי שיער.
מפת חשיבה: אטום
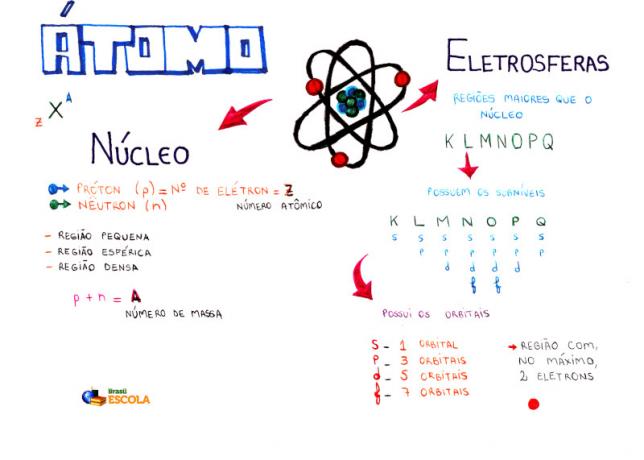
* להורדת מפת החשיבה ב- PDF, לחץ כאן!
בין המודלים האטומיים, הנפוץ ביותר כיום בתיכון להבנת מבנה האטום ותכונותיו הוא מודל רתרפורד-בוהר. על פי מודל זה, מבנה האטום מורכב משני חלקים עיקריים: ה הליבה וה אלקטרוספירה.

שני חלקים עיקריים במבנה האטום - אלקטרוספרה וגרעין
* הליבה: הוא מהווה את החלק המרכזי של האטום, הוא קומפקטי, מסיבי וצפוף מאוד, בנוסף להיותו נוצר על ידי חלקיקים בעלי מסה גדולה יותר, שהם פרוטונים ונויטרונים.

איור של הפרוטונים והנייטרונים המרכיבים את גרעין האטום
- פרוטונים: הם חלקיקים עם מטען חשמלי חיובי (מטען יחסי = +1; מטען בקולומב (C) = +1.602. 10-19) והמסה היחסית שלו שווה ל- 1.
העובדה שפרוטונים יוצרים את הגרעין ומעניקים לו מטען חיובי כולל התגלתה על ידי יוגן גולדשטיין, בשנת 1886, באמצעות שינוי באמפולה של קרוקוס וכמה ניסויים. הוא ראה שתחת מתחים גבוהים מאוד הופיעו פליטות (קרני האנודה - שרידי אטומי הגז שנמצאים בתוך הנורה ושהאלקטרונים שלהם נקרעו מהפריקה החשמלית). על ידי הצבת שדה חשמלי או מגנטי מחוץ לנורה, קרניים אלה הוסטו לעבר הקוטב השלילי. פירוש הדבר שהיו חלקיקים תת-אטומיים חיוביים שנקראו פרוטונים.
יותר מאוחר, ארנסט רתרפורד (1871-1937) ביצע את הניסוי המתואר בטקסט האטום של רתרפורד, מה שהוביל אותו לגלות את מיקום הפרוטון: בגרעין.
- נויטרונים: הם חלקיקים עם מסה השווה לזה של פרוטונים (1), אך כפי שהשם מרמז, הם ניטרליים, כלומר אין להם מטען חשמלי.
נויטרונים התגלו בשנת 1932 על ידי ג'יימס צ'דוויק (1891-1974), שהבין שגרעין הבריליום הרדיואקטיבי פולט חלקיקים נייטרליים עם מסה השווה בערך למסת הפרוטונים (למעשה, הוא גדול מעט יותר).
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
קוטר הגרעין תלוי בכמות הפרוטונים והנייטרונים שיש לאטום, אך בממוצע הוא נע סביב 10-14 חודש 10-15 M.
גרעין האטום מרכז כמעט את כל המסה של האטום, בהיותו חלק קטן מאוד: גם הפרוטון וגם הנויטרון קטנים פי 100,000 מכל האטום עצמו! לשם השוואה, דמיין שאנו מגדילים את גרעין האטום של היסוד מימן (שיש לו רק פרוטון) בגודל של כדור טניס, האלקטרון הקרוב ביותר יהיה כשלושה קילומטרים ממנו מֶרְחָק! גם אם אטום היה מוגדל לגובה של בניין בן 14 קומות, ליבתו תהיה בגודל של גרגר מלח בלבד בקומה השביעית. זה באמת משהו מדהים, אתה לא חושב ?!
* אלקטרוספרה: האם אזור שבו אלקטרונים מסתובבים סביב הגרעין. למרות היותו אזור בעל נפח גדול בהרבה מהגרעין, הוא כמעט ריק, מכיוון שכל אלקטרון קטן פי 1836 מפרוטון אחד (או מנויטרון אחד). זו הסיבה שמסת האטום כמעט כל היא בגרעין. אלקטרונים הם חלקיקים עם מטען חשמלי שלילי (-1).
אלקטרונים התגלו בשנת 1897 על ידי ג'וזף ג'ון תומסון (1856-1940), היוצר של מודל אטומי של תומסון. ניתן לראות את הניסוי של תומסון בפירוט בטקסט הניסוי של תומסון בפריקות חשמל, אך בקיצור, הוא השתמש באמפולה של קרוקוס הנ"ל והבין שקרני הקתודה הן תמיד נמשך על ידי הקוטב החיובי, שהוכיח שלאטום יש חלקיקים שליליים, שנקראו אלקטרונים.
אלקטרונים מסתובבים סביב הגרעין מיליארדי פעמים למיליון שנייה, מעצבים את האטום וגורמים לו להתנהג כאילו הוא מוצק.
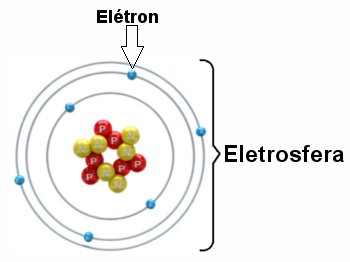
איור של אלקטרוספירה עם שלוש שכבות אלקטרוניות ואלקטרונים המסתובבים סביב הגרעין.
בקצרה, אנו יכולים ליצור טבלה להבדיל בין שלושת החלקיקים התת אטומיים העיקריים שהם חלק ממבנה האטום:

מסה ומטען חשמלי של שלושת החלקיקים התת אטומיים העיקריים - פרוטונים, נויטרונים ואלקטרונים
האטומים של כל היסודות הכימיים מורכבים משלושת החלקיקים התת אטומיים הללו. מה שמבדיל יסוד כימי אחד לאחר הוא הכמות בה מופיעים חלקיקים אלה, במיוחד כמות הפרוטונים בגרעין, הנקראת מספר האטום. המשך ללמוד על כך דרך הטקסט. יסוד כימי.
* מפת חשיבה מאתי. דיוגו לופס
מאת ג'ניפר פוגאצה
בוגר כימיה
כִּימִיָה
סיווג חומר, מים, גז הידרוציאני, פחמן דו חמצני, אמוניה, מימן, הליום, חומרים חומרים פשוטים, מורכבים, תערובות, שלבי תערובת, תערובת הומוגנית, תערובת הֵטֵרוֹגֵנִי.