החוק של דלטון קובע כי הלחץ החלקי של כל גז בתערובת גז שווה ללחץ שהיה מפעיל את נפח התערובת, באותה טמפרטורה. לכן, הלחץ הכולל של תערובת הגז הוא סכום הלחצים החלקיים של כל גז המרכיב אותו.
בואו ניקח בחשבון שני סוגים של גזים, A ו- B. כל אחד מהם תופס את אותו נפח V ויש לו את אותה הטמפרטורה T. אם אנו מיישמים את משוואת Clapeyron על שני הגזים A ו- B, יש לנו:
פה .V = nה .R .T ו- pב .V = nב .R .T
כפי שמוצג באיור לעיל, אם נערבב את שני הגזים, מספר השומות של הגזים בתערובת (לאM) זה הופך להיות:
לאM= nה+ nב
איפה:
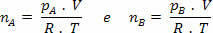
אבל nm = (Pm.V) / R. T; אז יש לנו:
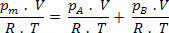
ביצוע כמה פשטות בביטוי לעיל, יש לנו:
פM= עמ 'ה+ עמ 'ב (חוק דלתון)
אנו יכולים להחיל את אותה הנמקה על גזים בעלי נפחים וטמפרטורות שונות. בואו נראה את הדמות למטה, בה שני בלונים המחוברים באמצעות צינור בעל נפח זניח הם בעלי ברז מגע. לבלונים אלה שני גזים A ו- B, הטמפרטורות והנפחים שונים זה מזה. מהאיור אנו רואים שהברז סגור, לכן:
פה .V = nה .R .T ו- pב .V = nב .R .T
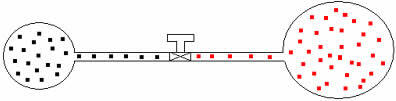
בהמשך, אם נפתח את הברז, נראה כי הגזים מתערבבים, כפי שמוצג באיור להלן:
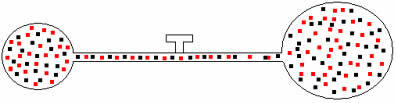
לתערובת זו יש לנו את היחסים הבאים:
וM= V.ה+ V.ב
פה .V = nה .R .T
פב .V = nב .R .T
אז יש לנו שניתן להרחיב את הקשר הסופי של תערובת זו לתערובת של לא גזים. לכן:
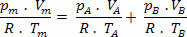
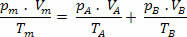
מאת דומיטיאנו מארקס
בוגר פיזיקה
צוות בית הספר בברזיל

