או חישוב מספר החלקיקים האטומיים משמש לציון כמות הפרוטונים (בגרעין), אלקטרונים (באלקטרוספרה) ונויטרונים (בגרעין) הקיימים בכל אטום או יון כלשהו. לשם כך, חשוב לדעת כמה מאפיינים של אטומים:
1- מספר אטומי (Z)
זהו קוד מתמטי המיוצג על ידי האות הגדולה Z, הממוקם בצד שמאל תחתון של קיצור האטום:
זאיקס
זה מציין את מספר הפרוטונים (p) בגרעין ואת מספר האלקטרונים (e) באלקטרוספרה של אטום. אז, באופן כללי:
Z = p = e
2- מספר מסה (A)
זהו קוד מתמטי המתאים לסכום מספר הפרוטונים (p) והניטרונים (n), שניהם נמצאים בגרעין של אטום כלשהו. המשוואה המייצגת את מספר המסה ניתנת על ידי:
A = p + n
מכיוון שמספר הפרוטונים שווה למספר האטומי, אנו יכולים לכתוב את המשוואה כדי לחשב את מספר המסה באופן הבא:
A = Z + n
אם אנו יודעים את מספר המסה והמספר האטומי של אטום, אנו יכולים לקבוע את מספר הנויטרונים באופן הבא:
n = A - Z
3- יונים
הם אטומים שמאבדים או צוברים אלקטרונים. יש להם סימן חיובי או שלילי הממוקם בפינה השמאלית העליונה של הייצוג שלהם, כמו במודל הבא:
איקס+ או X-
יון חיובי: זה נקרא קטיון והסימן החיובי מציין שהוא איבד אלקטרונים.
יון שלילי: זה נקרא אניון והסימן השלילי מציין שהוא צבר אלקטרונים.
אל תפסיק עכשיו... יש עוד אחרי הפרסום;)
4- דמיון אטומי
א) איזוטופים
אטומים שיש להם מספר אטומי זהה ומספרי מסה שונים. דוגמא:
7איקס14 ו 7י16
לאטומים X ו- Y אותו מספר אטומי (משמאל לראשי התיבות), כלומר שווה ל- 7. לאטום X יש מספר מסה (מימין לראשי התיבות) השווה ל- 14, ולאטום Y מספר מסה השווה ל -16.
ב) איזובארים
אטומים שיש להם מספר מסה זהה ומספרים אטומיים שונים. דוגמא:
15איקס31 ו 13י31
לאטומים X ו- Y מספר מסה (מימין לראשי התיבות) השווה ל- 31. לעומת זאת, אטום X הוא בעל מספר אטומי השווה ל -15, ובאטום Y מספר אטומי השווה ל- 13.
ג) איזוטונים
אטומים שיש להם מספר מסה ומספרים אטומיים שונים, אך אותו מספר נויטרונים.
ד) אלקטרואיזון
אטומים שיש להם מספר זהה של אלקטרונים. דוגמא:
12איקס+2 ו 7י-3
לאטום X מספר אטומי השווה ל- 12 והוא קטיון (עם מטען חיובי +2), ולכן הוא מאבד שני אלקטרונים, ובכך יש 10 אלקטרונים באלקטרוספירה שלו. לעומת זאת, אטום Y הוא בעל מספר אטומי השווה ל 7 והוא אניון (עם מטען שלילי -3), ולכן הוא צובר שלושה אלקטרונים ובכך יש לו 10 אלקטרונים באלקטרוספרה שלו.
מפת חשיבה: חלקיקים אטומיים
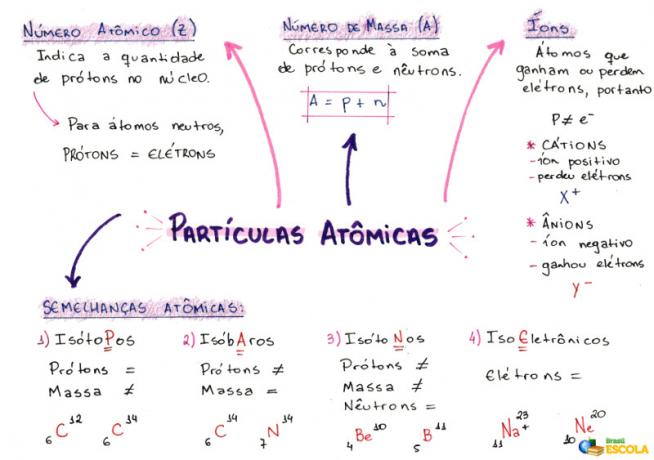
* להורדת מפת החשיבה ב- PDF, לחץ כאן!
דוגמאות לחישוב מספר החלקיקים האטומיים
דוגמה 1: קבע את מספר הפרוטונים, הנויטרונים והאלקטרונים באטום 14איקס29.
הערכים הבאים עבור אטום X ניתנו:
מספר המסה (ימני עליון) = 29
המספר האטומי (משמאל למטה) = 14
כדי לקבוע את מספר הפרוטונים:
מספר הפרוטונים תמיד שווה למספר האטומי, ולכן לאטום X יש 14 פרוטונים.
לקביעת מספר האלקטרונים:
מכיוון שהאטום X אינו יון, לכן מספר האלקטרונים שווה למספר הפרוטונים, כלומר 14.
לקביעת מספר הנייטרונים:
מספר הנויטרונים נקבע באמצעות מספר המסה והפרוטונים בנוסחה הבאה:
A = p + n
29 = 14 + n
29 - 14 = n
n = 15
דוגמה 2: קבע את מספר הפרוטונים, הנויטרונים והאלקטרונים של יון X+3, בידיעה שמספר המסה שלהם ומספרם האטומי הם בהתאמה 51 ו- 23.
הערכים הבאים עבור יון X ניתנו:
מספר מסה = 51
המספר האטומי (שמאל למטה) = 23
כדי לקבוע את מספר הפרוטונים:
מספר הפרוטונים תמיד שווה למספר האטומי, ולכן באטום X יש 23 פרוטונים.
לקביעת מספר האלקטרונים:
היון X חיובי (+3), ולכן זהו קטיון שאיבד שלושה אלקטרונים. אז מספר האלקטרונים שלו הוא 20.
הערה: הפחתה או עלייה במספר האלקטרונים מתרחשת תמיד ביחס למספר האטומי.
לקביעת מספר הנייטרונים:
מספר הנויטרונים נקבע באמצעות מספר המסה והפרוטונים בנוסחה הבאה:
A = p + n
51 = 23 + n
51 - 23 = n
n = 28
דוגמה 3: לאטום W יש מספר אטומי ומסה השווה, בהתאמה, 29 ו -57, בהיותו איזון של a אטום Y, שיש לו מספר אטומי השווה ל- 30, שהוא איזוטופ של אטום B, שמספרו המסה הוא 65. בעזרת מידע זה, קבע את מספר הפרוטונים, הנויטרונים והאלקטרונים באטום B.
הנתונים שנמסרו על ידי התרגיל:
אטום W.
מספר אטומי (למטה משמאל) = 29
מספר המסה (ימני עליון) = 57
איזובאר Y, כלומר המסה של Y היא גם 57.
אטום Y
מספר אטומי = 30
מספר מסה = 57
עם שני הערכים הללו, עלינו לקבוע את מספר הנויטרונים שלו מכיוון שהוא איזוטון של יסוד B:
A = Z + n
57 = 30 + n
57 - 30 = n
n = 27
קבר:
מספר מסה = 65
מספר הנויטרונים = 27
עם נתונים אלה עלינו לקבוע את מספר האטום שלו, מכיוון שעם זה נקבע את מספר הפרוטונים שלו ואת מספר האלקטרונים שלו (מכיוון שהוא אינו יון):
A = Z + n
65 = Z +27
65 - 27 = Z
Z = 38
לכן באטום B יש 38 פרוטונים, 38 אלקטרונים ו- 27 נויטרונים.
* מפת חשיבה מאת ויקטור ריקרדו פריירה
מורה לכימיה
על ידי. דיוגו לופס דיאס