או נתרן כלורי (מלח שולחן) הוא המלח שאנו משתמשים בו בחיי היומיום שלנו למלח מזון בעבודת יד או מעובד (מתועש). זהו חומר שקיים גם במזונות טבעיים שונים הנצרכים על ידינו על בסיס יומיומי, כגון פירות, ירקות, קטניות, זרעים וכו '.
בטקסט זה תוכלו לדעת הכל על החומר החשוב הזה לחיי היומיום של האדם:
ההגדרה
נתרן כלורי שייך לתפקוד האורגני של מלחים והוא מורכב מקשר הקטיון הנתרן (Na+) זה ה אניון גשםאורטו (קל-) דרך א קשר יוני.
ב) מאפיינים כימיים
נתרן כלורי נוצר על ידי שני יסודות כימיים:
→ נתרן (Na):
שייך למשפחת המתכות (המסוגלת ליצור קטיונים בקלות) אלקליין (AI);
בעל אלקטרון במעטפת הערכיות;
יש מספר אטומי השווה ל 11;
בעל אלקטרופוזיביות גבוהה (יכולת לאבד אלקטרונים).
→ כלור (Cl)
שייך למשפחת ההלוגנים (VIIA);
זה לא מתכתי (בגלל זה הוא הופך לאניון כל כך בקלות);
בעל שבעה אלקטרונים במעטפת הערכיות;
יש מספר אטומי השווה ל 17;
בעל אלקטרונגטיביות גבוהה (יכולת להשיג אלקטרונים).
כשני היסודות הכימיים היוצרים נתרן כלורי נוכחים, בהתאמה, חשמלית גבוהה וגבוהה אלקטרגטיביות, ביניהם קיים קשר יוני (שנוצר בין אטומים עם נטייה לאבד ולהרוויח אלקטרונים).
המבנה הכימי של נתרן כלורי מורכב מאניון כלורי יחיד (כדור ירוק), אשר מתקשר עם שישה קטיונים של נתרן (כדורים כחולים), כפי שניתן לראות במבנה להלן:
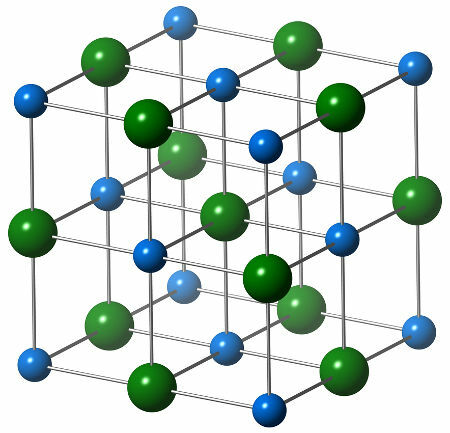
ייצוג מבנה הגביש של נתרן כלורי
ג) מאפיינים פיזיים
נקודת היתוך:
ניתן להפוך נתרן כלורי ממצב מוצק למצב נוזלי בטמפרטורה של 801 אוÇ.
נקודת רתיחה:
ניתן להפוך נתרן כלורי מנוזל למצב גזי בטמפרטורה של 1465 אוÇ.
קוטביות
מכיוון שמדובר בחומר שמקורו בקשר יוני, כלומר מכיוון שהוא תרכובת יונית, נתרן כלורי הוא קוטבי.
מסיסות במים
אנחנו יכולים להתמוסס ב 1 ליטר מים, בגיל 25 אוC, עד 359 גרם נתרן כלורי.
מסיסות בממיסים אחרים:
מאחר ונתרן כלורי הוא תרכובת קוטבית, לא ניתן להמיס בשום ממס בעל אופי לא קוטבי, כגון שמן.
צְפִיפוּת:
הצפיפות של נתרן כלורי היא 2.165 גרם / מ"ל, ולכן היא צפופה יותר ממים, שצפיפותם שווה ל- 1 גרם / מ"ל.
מוליכות חשמלית:
מכיוון שמדובר בתרכובת יונית, נתרן כלורי מסוגל להוביל זרם חשמלי רק כאשר:
הוא נמצא במצב מותך, כלומר נוזלי;
מומס במים.
ד) שיטות השגה
ניתן להשיג נתרן כלורי פיזית או כימית:
1אומתחיל להיות פיזי:
התגבשות חלקית
נתרן כלורי מתקבל על ידי אידוי מים מהאוקיאנוסים.
מוקשים תת קרקעיים
הוא מופק במכרות באמצעות טכניקות כרייה.
פיקדונות תת קרקעיים
הוא מופק משקעים תת קרקעיים עמוקים על ידי התמוססות במים (המלח הקיים במאגר מתמוסס) ובעקבותיו שאיבה.
2או) להשיג כימית
תגובת סינתזה
ניתן להשיג נתרן כלורי מתגובה כימית של סינתזה (חומרים פשוטים מולידים חומר מורכב) בין גז כלור לנתרן מתכתי:
2 ב(ים) + קל2 (גרם) → 2 NaCl(ים)
תגובת ניטרול:
דרך נוספת להשיג נתרן כלורי כימית היא באמצעות תגובת ניטרול בין חומצה הידרוכלורית לנתרן הידרוקסיד, בה יש לנו היווצרות מלח ומים:
HCl(1) + NaOH(פה) → NaCl(פה) + H2או(1)
ה) חשיבות לבני אדם
נתרן כלורי בפני עצמו אין תפקיד בגוף האדם, אך כאשר הוא מתנתק לקטיוני נתרן (Na+) ואניוני כלוריד (Cl-), לכל אחד משני היונים הללו יש כמה פונקציות חשובות לגופנו. ראה כמה מהפונקציות הבאות:
→ פונקציות של קטיון הנתרן (Na+)
מונע קרישת דם;
נלחם ביצירת כליות ואבני מרה;
משתתף בוויסות נוזלי הגוף;
משתתף בוויסות לחץ הדם.
→ פונקציות של האניון הכלורי (Cl-)
השתתפות בהיווצרות והרכבת מיץ קיבה (חומצה הידרוכלורית - HCl);
השתתפות ביצירת מיץ לבלב.
ו) נזק לגוף האדם
צריכה מוגזמת של נתרן כלורי יכולה לגרום לפגיעה הבאה בבני אדם:
→ נזק הנגרם כתוצאה מכמות יתר של נתרן בגוף:
זמן ריפוי פצעים מוגבר;
שכיחות מוגברת של התכווצויות;
לחץ דם מוגבר;
עומס יתר על הכליות;
החזקת נוזלים מוגברת בגוף.
→ נזק שנגרם מעודף אניוני כלוריד בגוף:
הרס של ויטמין E;
ירידה בייצור יוד בגוף.
ז) יישומים אחרים
בנוסף לשימוש במלח אוכל, ניתן להשתמש בנתרן כלורי גם במצבים הבאים:
ייצור שמפו;
ייצור נייר;
ייצור של נתרן הידרוקסידי (NaOH);
ייצור חומרי ניקוי;
ייצור סבונים;
שלג נמס במקומות הסובלים מסופות שלג;
ייצור נתרן מתכתי;
ייצור גז כלור;
באיזוטוניקה להחלפת אלקטרוליטים בגוף;
בתמיסות נוגדות-דלקת באף;
ייצור תמיסת מלח; בין שאר היישומים.
על ידי. דיוגו לופס דיאס