היכולת שיש לחיבורים למשוך מטענים חשמליים מוגדרת כקוטביות, שמקבלת אופי שונה בהתאם לחיבור בו הוא קיים.
לגבי הקשר היוני והקוולנטי, האחרון הופך את המולקולה ללא קוטבית. המולקולה שבה הקשר היוני אחראי על קיום אטומים זה לזה יש קוטביות.
הקשר השולט בין תרכובות אורגניות הוא קוולנטי, ולכן הם הופכים לרוב לתרכובות לא קוטביות. שרשראות הפחמן הארוכות הקיימות בחומרים אורגניים אינן מאפשרות להן שום אופי אחר שאינו קוטביות.
ההסבר נובע מכך שהקשר מתרחש בין אלמנטים שווים (Ç-Ç), לכן יש להם את אותו סולם אלקטרונטיבי. ראה דוגמה:

מולקולה לא קוטבית
הבוטאן המיוצג על ידי המבנה לעיל הוא גז, שימו לב כי אטומי הקשר הם זהים (4 פחמנים קשורים זה לזה).
אך אין זה אומר שכל תרכובת אורגנית אינה קוטבית, הימצאותם של אטומים אחרים בין פחמנים מעניקה למולקולה אופי קוטבי. בדוק את הדוגמה:
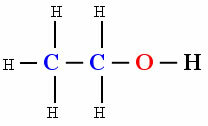
מולקולה קוטבית
נוכחות של הידרוקסיל הו (חמצן המקושר למימן) גרם למולקולת התרכובת האורגנית אתנול להראות קוטביות.
בוטאן משמש כגז למצתים ואתנול הוא מה שנקרא אלכוהול נפוץ.
מאת ליריה אלבס
בוגר כימיה
צוות בית הספר בברזיל
ראה עוד!
תכונות של תרכובות אורגניות
קוטביות – גלה מדוע אלקטרונגטיביות משפיעה על קוטביות השיחה.
קוטביות של קשרים יוניים וקוולנטיים
כימיה אורגנית - כִּימִיָה - בית ספר ברזיל
מָקוֹר: בית ספר ברזיל - https://brasilescola.uol.com.br/quimica/polaridade-dos-compostos-organicos.htm
