oh Diagramma delle fasi è un grafico utilizzato per indicare le condizioni di temperatura e pressione necessario per ottenere un sostanza in un certo stato fisico (solido, liquido o gassoso).
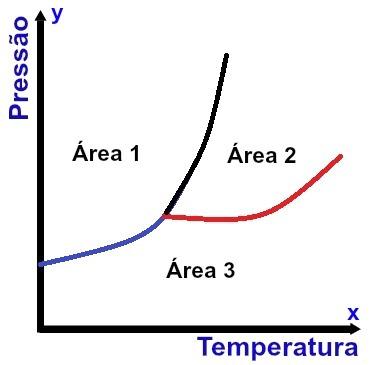
Rappresentazione di un diagramma di fase
L'asse x (orizzontale) contiene i valori di temperatura e l'asse y (verticale) contiene i valori di pressione. Inoltre, sono presenti tre curve collegate ad un unico punto (detto punto triplo), che dividono il grafico in tre aree ben definite, come si vede nel diagramma sopra riportato.
Oltre a indicare le condizioni affinché la sostanza si trovi in uno specifico stato fisico, il Diagramma delle fasi indica le condizioni affinché si verifichi qualsiasi cambiamento nello stato fisico.
I cambiamenti nello stato fisico sono:
Fusione: passaggio dallo stato solido allo stato liquido;
solidificazione: passaggio dallo stato liquido allo stato solido;
Vaporizzazione: passaggio dallo stato liquido allo stato gassoso;
Condensazione: passaggio dallo stato gassoso allo stato liquido;
sublimazione: passaggio dallo stato solido allo stato gassoso;
Risublimazione: passaggio da gas a stato solido.
a) Regioni
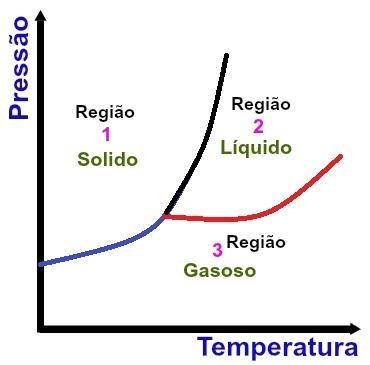
Regioni fondamentali di un diagramma di fase
Regione 1
La regione 1 indica le condizioni di temperatura e pressione in cui troviamo la sostanza allo stato solido.
Regione 2
La regione 2 indica le condizioni di temperatura e pressione in cui troviamo la sostanza allo stato liquido.
Regione 3
La regione 3 indica le condizioni di temperatura e pressione in cui troviamo la sostanza allo stato gassoso.
b) Curve

Curve presenti in un diagramma di fase
Curva A (curva viola)
È la curva che divide la regione solida e gassosa del diagramma di fase ed è comunemente chiamata curva di risublimazione. Ogni punto situato sulla curva 1 indica che abbiamo una certa sostanza che coesiste allo stato solido e gassoso.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
La curva 2, oltre a indicare la coesistenza, indica anche le condizioni di temperatura e pressione per la trasformazione di una sostanza da uno stato liquido a uno gassoso.
Curva B (curva nera)
È la curva che divide la regione solida e liquida del diagramma di fase ed è comunemente chiamata curva di solidificazione. Ogni punto situato sulla curva 2 indica che abbiamo una certa sostanza che coesiste allo stato solido e gassoso.
Oltre a indicare la coesistenza, la curva 2 indica anche le condizioni di temperatura e pressione per la trasformazione di una sostanza dallo stato liquido allo stato solido.
Curva C (curva rossa)
È la curva che divide la regione solida e gassosa del diagramma di fase ed è comunemente chiamata curva di condensazione. Ogni punto situato sulla curva 3 indica che abbiamo una certa sostanza che coesiste allo stato solido e gassoso.
Oltre a indicare la coesistenza, la curva 3 indica anche le condizioni di temperatura e pressione per la trasformazione di una sostanza da uno stato solido a uno gassoso e viceversa.
c) Il punto triplo
Il punto in cui si incontrano le tre curve nel diagramma di fase è chiamato punto triplo. A questo punto abbiamo il valore di temperatura e il valore di pressione al quale troviamo la sostanza allo stato solido, liquido e gassoso contemporaneamente.

d) Cambiamenti di stato fisico nel diagramma di fase
Nel diagramma di fase sottostante, abbiamo 6 frecce che indicano la direzione dei cambiamenti negli stati fisici di una sostanza.

Freccia 1: indica la fusione
Freccia 2: indica la solidificazione
Freccia 3: indica la vaporizzazione
Freccia 4: indica la condensa
Freccia 5: indica la sublimazione
Freccia 6: indica la sublimazione
Di Me. Diogo Lopes Dias
Vorresti fare riferimento a questo testo in un lavoro scolastico o accademico? Guarda:
GIORNI, Diogo Lopes. "Cos'è un diagramma di fase?"; Brasile Scuola. Disponibile in: https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-diagrama-fases.htm. Consultato il 28 giugno 2021.
Chimica

Trasformazioni liquide, evaporazione, forze intermolecolari, supercongelamento liquido, cristallizzazione liquida, tempra, viscosità del liquido, pressione di vapore del liquido, pressione atmosferica, congelamento di liquidi, temperatura
Chimica

Liquidi, tensione superficiale, fusione di un solido, condensazione di un gas, viscosità, fluido, volume costante, molecole di un gas, forze intermolecolari, compressione, evaporazione di un liquido.