Per classificare un collegamento sigma, è fondamentale saperlo riconoscere nella struttura di una molecola. Il legame sigma è in realtà un legame covalente che si verifica quando due orbitali atomici incompleti (con un solo elettrone) compenetrano sullo stesso asse. Un esempio è quando un orbitale di tipo p (elica) si compenetra con un altro orbitale p.

orbitali p che si compenetrano in un legame p-p sigma
In pratica (negli esercizi), il riconoscimento e la classificazione di un collegamento sigma avviene dalla formula di struttura di una sostanza, come nella rappresentazione strutturale di seguito:

Formula di struttura dell'acido cianidrico
Prima di classificare un collegamento sigma, è necessario saperlo riconoscere in una formula di struttura. Per questo, ricorda solo il modi come un legame covalente è rappresentato: la chiamata semplice è rappresentato da un singolo trattino (-), il paio è rappresentato da due (=) e il collegamento triplicare è rappresentato da tre (≡). Il legame sigma è presente in una delle tre rappresentazioni dei legami covalenti come segue:
Semplice: ha un legame sigma;
Paio: Dei due collegamenti, solo uno è sigma;
Triplicare: Uno dei tre collegamenti è sigma.
Sapendo come riconoscere un link sigma, il passo successivo è imparare a classificarlo. Per questo, dobbiamo sapere qual è l'orbitale incompleto di ciascun atomo coinvolto nel legame:
H - presenta l'orbitale s incompleto, quindi, nella classificazione, è rappresentato da s.
Ametals- hanno un orbitale p incompleto, quindi, nella classificazione, sono rappresentati da p, ad eccezione dei seguenti elementi:
Carbonio: Il tuo orbitale incompleto dipende dal tipo di ibridazione che soffre. Le possibilità sono: ibridazione sp3 (quanto fa quattro semplici chiamate), sp2 (quanto fa due legami singoli e uno doppio) o sp (quanto realizza due doppi legami o uno singolo e uno triplo). Pertanto, nella classificazione di un legame sigma, il carbonio può essere rappresentato da sp3, sp2 o sp a seconda della chiamata che stai effettuando.
Berillio:soffrire ibridazione di tipo sp, quindi, nella classificazione, è rappresentato da sp.
Boro:soffrire ibridazione di tipo sp2, quindi, nella classificazione, è rappresentato da sp.2.
Con tutte queste informazioni, la parte più semplice è classificare i collegamenti sigma presenti in una struttura. Vediamo alcuni esempi:
Esempio 1: connessioni sigma in acqua

Formula strutturale dell'acqua
La formula strutturale sopra mostra che l'acqua ha due legami sigma (due semplici), essendo loro tra l'ossigeno (rappresentato da p) è il Idrogeno (rappresentato da s). Pertanto, abbiamo due collegamenti sigma classificati in:
s-p
Esempio 2: Legami sigma nel tricloruro di fosforo

Formula strutturale del tricloruro di fosforo
La formula strutturale sopra mostra che il tricloruro di fosforo ha tre chiamatesigma (tre semplici), essendo loro entra nel fosforo (rappresentato da p) è il cloro (rappresentato da p). Pertanto, abbiamo tre collegamenti sigma classificati in:
p-p
Esempio 3: legami sigma nel trifluoruro di boro
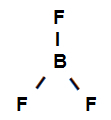
Formula di struttura del trifluoruro di boro
La formula strutturale sopra mostra che il trifluoruro di boro ha tre link sigma (tre semplici), essendo loro entra nel boro (rappresentato da sp2) è il Fluoro (rappresentato da p). Pertanto, abbiamo tre collegamenti sigma classificati in:
p-sp2
Esempio 4: legami sigma in etanolo
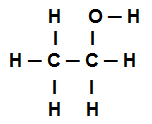
Formula strutturale dell'etanolo
La formula strutturale per l'etanolo sopra mostra che abbiamo la presenza di otto chiamate sigma (otto semplici collegamenti). Sono loro:
Uno tra gli Ossigeno (rappresentato da p) e l'idrogeno (rappresentato da s). Pertanto, il collegamento è classificato in sigma s-p.
Uno dei due carboni che eseguono solo connessioni sigma (e quindi rappresentato da sp3). Pertanto, il collegamento è classificato in sp3-P3.
Uno tra i Carboni (rappresentato da sp3) e l'ossigeno (rappresentato da p). Pertanto, il collegamento sigma è classificato in p-sp3.
cinque tra carbonio (rappresentato da sp3) e l'idrogeno (rappresentato da s). Quindi, tutti e cinque sono classificati in s-sp3.
Esempio 5: Sigma bond nel dicloroetene

Formula di struttura del dicloroetene
La formula strutturale di Dicloroetene sopra mostra che abbiamo la presenza di cinque link sigma (i quattro legami singoli e uno dei doppi legami). Sono loro:
Uno dei due carboni che eseguono due legami singoli e uno doppio (e quindi rappresentato da sp2). Pertanto, il collegamento sigma è classificato in sp2-P2.
Quattro sono tra il carbonio(rappresentato da sp2)e l'idrogeno (rappresentato da s). Quindi, tutti e quattro sono classificati in s-sp2.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/classificacao-uma-ligacao-sigma.htm
