oh benzene è un composto organico classificato come a idrocarburo aromatico. È ampiamente utilizzato come materia prima nelle industrie, nei processi di laboratorio, nelle aziende siderurgiche e nelle industrie petrolchimiche per la raffinazione del petrolio.
Leggi anche: Metano: il più piccolo e semplice degli idrocarburi
Formula
Il benzene è un composto di formula molecolare Ç6H6e chi ha un struttura estremamente stabilel. La formula strutturale del benzene è rappresentata come segue:
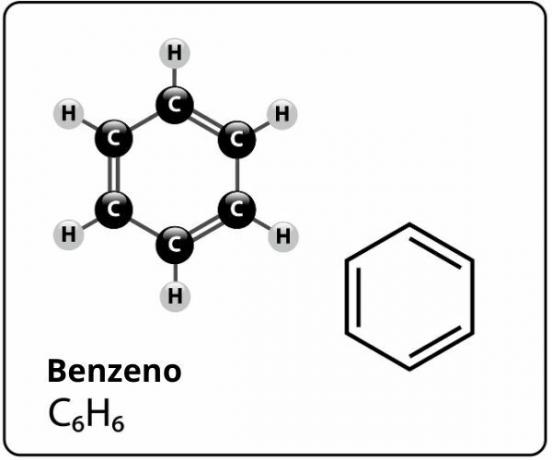
Chi ha proposto questa struttura per il benzene con sei atomi di carbonio legati insieme con doppi legami alternati, formando un esagono e avendo attaccato a ciascuno di essi un atomo di idrogeno, era il chimico tedesco Friedrich August Kekule, nel 1866.
Il benzene subisce un fenomeno chiamato risonanza, in cui gli elettroni nei legami tra i carboni differiscono nella loro posizione. Per questo motivo, il benzene può essere rappresentato come segue:
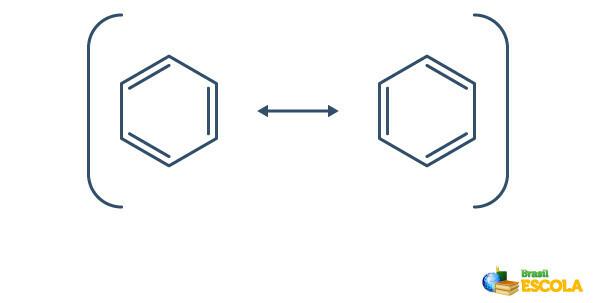
La struttura effettiva del benzene è un intermediario tra le strutture di risonanza mostrate sopra. Ciò non significa che il benzene a volte appaia in una forma, a volte nell'altra, né che entrambe le forme esistano contemporaneamente. Rappresentiamo il benzene come segue:
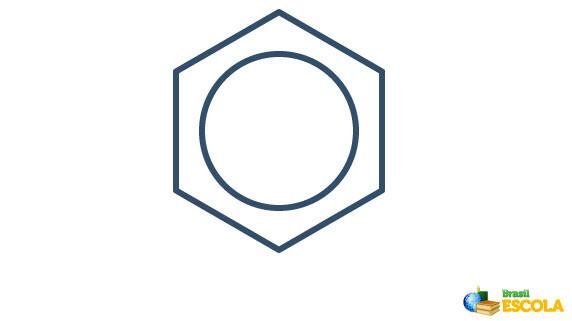
Il cerchio all'interno dell'esagono rappresenta la risonanza tra gli elettroni nei legami.
Caratteristiche
- Il benzene è un liquido incolore, infiammabile è comune aroma gradevole caratteristica.
- Formula molecolare: C6H6.
- Massa molare: 78,11 g/mol.
- Densità: 0,876 g/cm³.
- Temperatura di fusione: 5,5 °C.
- Temperatura di ebollizione: 80,1 ºC – la sua bassa temperatura di ebollizione spiega la sua elevata volatilità (facilità di evaporazione).
Il benzene è un sostanza tossica e i suoi vapori possono causare vertigini, mal di testa e svenimenti.
Leggi anche:Monossido di carbonio — gas estremamente tossico, incolore e inodore
Applicazioni e tossicità del benzene
il benzene è utilizzato principalmente come materia prima nelle industrie per la produzione di altre sostanze, come materie plastiche e polimeri a base di stirene, resine, adesivi, nylon, gomme, lubrificanti, pesticidi, ecc.
Il benzene è stato sostituito, principalmente nei laboratori, dal toluene, che ha polarità e solubilità simili a quelli del benzene, ma è meno tossico e con una temperatura di ebollizione più elevata.
Il benzene fa parte del gruppo di group sostanze chimiche considerate cancerogene, causando danni al midollo osseo e leucemia, se esposto a lungo termine ad alte concentrazioni. A breve termine, il benzene può causare vertigini, sonnolenza, battito cardiaco accelerato, convulsioni e svenimenti.
Essendo un liquido volatile, il benzene rilascia facilmente gas e, quindi, la contaminazione da benzene avviene principalmente attraverso le vie respiratorie.
Dove si trova il benzene?
La maggior parte del benzene rilasciato nell'ambiente risulta dall'azione umana, principalmente nelle attività industriali, ma può anche essere rilasciato come sottoprodotto di incendi e attività vulcaniche.
il benzene è una delle sostanze costituenti di Petrolio ed è presente nella benzina, essendo rilasciato nell'atmosfera bruciando carburanti per automobili. Inoltre, si trova anche nelle bibite e nelle sigarette.

Polarità
Il benzene è un molecola non polare, proprio come tutti gli altri Idrocarburi e quindi presenta bassissima solubilità in acqua (0,8 g/L a 15°C). In alcune procedure di laboratorio, il benzene viene utilizzato come solvente organico per sostanze non polari.
Nomenclatura
Esiste una regola applicata solo alla nomenclatura dei composti aromatici, cioè quelli che hanno il benzene nella loro struttura. Questa regola è divisa in due casi, che dipendono dalla quantità di radicali attaccati all'anello benzenico.
1° CASO: quando c'è un solo radicale attaccato all'anello benzenico, il nome è dato seguendo la seguente regola:
NOME RADICALE + BENZENE
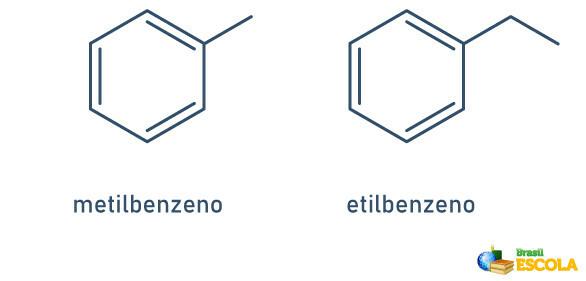
Si noti che non è necessario indicare la posizione dello stelo.
2° CASO: quando c'è più di un radicale attaccato al benzene, il nome segue la seguente regola:
POSIZIONE RADICALE + NOME RADICALE + BENZENE
Vedi l'esempio:

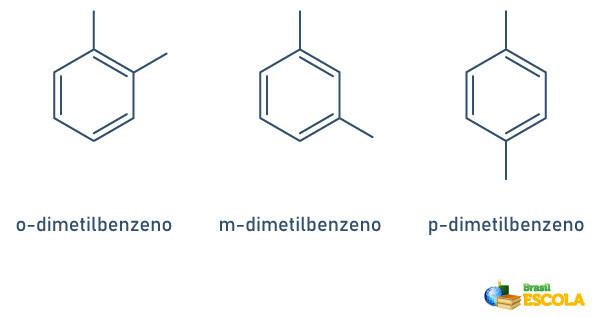
Quando l'anello benzenico ha solo due radicali attaccati, esiste una nomenclatura specifica che può essere utilizzata:
- 1,2 o orto(o);
- 1.3 o obiettivo (m);
- 1.4 o a (p).
Guarda gli esempi:
Leggi anche: Nitrato di ammonio — composto altamente reattivo utilizzato nella fabbricazione di esplosivi
curiosità
- Il benzene è una sostanza estremamente cancerogena, classificata dall'Agenzia Internazionale della ricerca sul cancro, nel Gruppo 1, insieme a tabacco, fumo diesel e carne elaborato.
- Esistono diversi organismi di regolamentazione che limitano l'esposizione e l'emissione di benzene in diversi paesi. In Brasile questo ruolo è di competenza di Anvisa.
- Prima di conoscerne i rischi, il benzene veniva utilizzato nei cosmetici, come il dopobarba, per il suo odore gradevole.
Di Victor Ricardo Ferreira
Insegnante di chimica
