entropia è la misura del grado di disordine di un sistema, essendo una misura dell'indisponibilità di energia.
È una grandezza fisica che è correlata a Seconda Legge della Termodinamica e che tende ad aumentare naturalmente nell'Universo.
Definizione di entropia
Il “disordine” non va inteso come “disordine” ma piuttosto come una forma di organizzazione del sistema.
Il concetto di entropia è talvolta applicato in altre aree del sapere con questo senso di disordine, che è più vicino al senso comune.
Ad esempio, immaginiamo tre vasetti, uno con piccole biglie blu, un altro con lo stesso tipo di biglie ma rosse, e il terzo vuoto.
Prendiamo il vaso vuoto e mettiamo tutte le palline blu sotto e tutte le palline rosse sopra. In questo caso, le palline sono separate e organizzate per colore.
Quando si agitava la pentola, le palline iniziavano a mescolarsi in modo tale che in un dato momento non ci fosse più la separazione iniziale.
Anche se continuiamo a scuotere il piatto, è improbabile che le palle tornino alla stessa organizzazione iniziale. Cioè, il sistema ordinato (palline separate per colore) è diventato un sistema disordinato (palline miste).

Quindi, la tendenza naturale è quella di aumentare il disordine di un sistema, il che significa un aumento dell'entropia. Possiamo allora dire che nei sistemi: ΔS >0, dove S è l'entropia.
Capisci anche di cosa si tratta entalpia.
Entropia e Termodinamica
Il concetto di Entropia iniziò ad essere sviluppato dall'ingegnere e ricercatore francese Nicolas Sadi Carnot.
Nella sua ricerca sulla trasformazione dell'energia meccanica in termica, e viceversa, scoprì che sarebbe impossibile che ci fosse una macchina termica pienamente efficiente.
IL Prima Legge della Termodinamica fondamentalmente determina che "l'energia è conservata". Ciò significa che nei processi fisici l'energia non viene persa, viene convertita da un tipo all'altro.
Ad esempio, una macchina utilizza energia per svolgere il lavoro e in tale processo la macchina si riscalda. Cioè, l'energia meccanica viene degradata in energia termica.
L'energia termica non si ritrasforma in energia meccanica (se ciò accadesse la macchina non si arresterebbe mai), quindi il processo è irreversibile.
Successivamente, Lord Kelvin ha completato la ricerca di Carnot sull'irreversibilità dei processi termodinamici, dando origine ai fondamenti di Seconda Legge della Termodinamica.
Rudolf Clausius fu il primo ad usare il termine Entropia nel 1865. L'entropia sarebbe la misura della quantità di Energia termica che non può essere convertita in energia meccanica (non può fare lavoro) a una certa temperatura.
Clausius ha sviluppato la formula matematica per la variazione dell'entropia ()S) attualmente utilizzata.
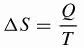
Essere,
ΔS: variazione di entropia (J/K)
Q: trasferimento di calore (J)
T: temperatura (K)
Leggi anche tu:
- Termodinamica
- Ciclo di Carnot
- Energia
- Tipi di energia
- Formule di fisica
Esercizi risolti
1) Enem - 2016
Fino al 1824 si riteneva che i motori termici, esempi dei quali sono i motori a vapore e gli attuali motori a combustione, potessero avere un funzionamento ideale. Sadi Carnot ha dimostrato l'impossibilità di una macchina termica, operante in cicli tra due sorgenti termiche (una calda e una fredda), di ottenere il 100% di efficienza. Tale limitazione si verifica perché queste macchine
a) eseguire lavori meccanici.
b) produrre un aumento dell'entropia.
c) utilizzare trasformazioni adiabatiche.
d) contravvenire alla legge sul risparmio energetico.
e) operare alla stessa temperatura della sorgente calda.
Alternativa: b) produrre un aumento dell'entropia.
2) Enem - 2011
Un motore può funzionare solo se riceve una quantità di energia da un altro sistema. In questo caso, l'energia immagazzinata nel combustibile viene, in parte, ceduta durante la combustione affinché l'apparecchio possa funzionare. Quando il motore è in funzione, parte dell'energia convertita o trasformata nella combustione non può essere utilizzata per svolgere il lavoro. Ciò significa che c'è una perdita di energia in un'altra forma. Carvalho, A. X. Z.
Fisica Termica. Belo Horizonte: Pax, 2009 (adattato).
Secondo il testo, le trasformazioni energetiche che si verificano durante il funzionamento del motore sono dovute ad a
a) è impossibile il rilascio di calore all'interno del motore.
b) il lavoro svolto dal motore è incontrollabile.
c) la conversione completa del calore in lavoro è impossibile.
d) la trasformazione dell'energia termica in cinetica è impossibile.
e) il potenziale utilizzo energetico del combustibile è incontrollabile.
Alternativa: c) la conversione completa del calore in lavoro è impossibile.
Vedi anche: Esercizi di Termodinamica