Utilizzando un'ampolla di Crookes, cioè tubi di vetro chiusi con un elettrodo positivo e uno negativo, contenenti gas a pressioni estremamente basse; lo scienziato inglese Joseph John Thomson (1856-1940) fece una scoperta essenziale per l'evoluzione del modello atomico.
Ha sottoposto questi gas a tensioni estremamente elevate, quindi è stato possibile osservare la comparsa di emissioni, che sono state chiamate raggi catodici. Quindi, è stato posto un campo elettrico esterno e, infine, è stato verificato che il raggio catodico è stato deviato, andando sempre nella direzione e direzione della piastra caricata positivamente. Pertanto, queste emissioni avevano oneri negativi.
Un altro punto importante è che indipendentemente dal gas utilizzato, era sempre lo stesso; così Thomson giunse alla logica conclusione che queste cariche negative erano presenti in qualsiasi materia, ne erano parte integrante. Fu così dimostrato che, contrariamente a quanto affermato da Dalton, l'atomo non era indivisibile, in quanto aveva una particella subatomica negativa, che prendeva il nome di
In sequenza, nel 1886, un altro scienziato, di nome Eugen Goldstein, scoprì la raggi anodici o canali, che erano raggi carichi positivamente, formati da ciò che restava degli atomi del gas a cui erano stati strappati gli elettroni dalla scarica elettrica. Questi raggi erano noti per possedere Carica positiva perché sono stati deviati nella direzione opposta ai raggi catodici, cioè sono stati attratti dalla piastra negativa.
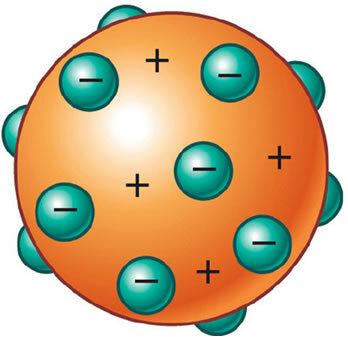
Si scoprì poi che l'atomo aveva anche una parte positiva, necessaria addirittura per mantenere la sua neutralità elettrica. Così, J. J. Thomson propose un nuovo modello per l'atomo, soprannominato il "budino all'uvetta" o "budino di prugne". Sarebbe una sfera non massiccia carica positivamente incrostata di elettroni (negativi) in modo che la sua carica elettrica totale sia nulla.
di Jennifer Fogaça
Laureato in Chimica
Squadra scolastica brasiliana
Chimica generale - Chimica - Brasile Scuola
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/quimica/o-experimento-thomson-com-descargas-eletricas.htm
