UN seconda legge della termodinamica determina quali condizioni esistono per il Calore essere convertiti in lavoro nei motori termici e nei frigoriferi. Affronta anche la definizione di entropia come fenomeno capace di misurare la disorganizzazione delle particelle nei sistemi fisici.
Leggi anche: Calorimetria: la branca della fisica che studia lo scambio termico
Argomenti di questo articolo
- 1 - Riassunto della seconda legge della termodinamica
- 2 - Qual è la seconda legge della termodinamica?
-
3 - Applicazioni della seconda legge della termodinamica
- Seconda legge della termodinamica nei motori termici
- Seconda legge della termodinamica nei frigoriferi
- 4 - L'entropia e la seconda legge della termodinamica
-
5 - Formule della seconda legge della termodinamica
- Macchine termiche e frigoriferi
- Frigoriferi
- Esempi di applicazione di formule
- 6 - Ciclo di Carnot
- 7 - Leggi della termodinamica
- 8 - Esercizi risolti sulla seconda legge della termodinamica
Riassunto sulla seconda legge della termodinamica
La seconda legge della termodinamica è rappresentata dalle affermazioni di Clausius e Kelvin-Planck.
L'affermazione di Clausius riguarda il flusso di calore dal corpo più caldo al corpo più freddo.
La dichiarazione di Kelvin-Planck affronta l'incapacità dei dispositivi termici di convertire tutto il loro calore in lavoro.
La seconda legge della termodinamica si applica ai motori termici e ai frigoriferi.
Il ciclo di Carnot è il ciclo di massima efficienza ottenuto dai motori termici.
Il ciclo di Carnot ha quattro fasi, un'espansione isoterma reversibile, un'espansione adiabatica reversibile, una compressione isoterma reversibile e una compressione adiabatica reversibile.
Il teorema di Carnot si riferisce al rendimento di Macchine di Carnot.
Qual è la seconda legge della termodinamica?
La seconda legge della termodinamica è a legge che affronta i vincoli che si verificano nei processi termodinamici. Fu enunciato dai fisici Rudolf Clausius (1822-1888), Lord Kelvin (1824-1907) e Max Planck (1858-1947), come vedremo in seguito:
Il fisico e matematico Rudolf Clausius ha affermato che il flusso di conduzione del calore avviene dal corpo a temperatura più alta a quello a temperatura più bassa. temperatura più bassa, quindi, non è naturale che avvenga il processo inverso, quindi, è necessario lavorare su questo sistema. Con ciò, ha affermato:
È impossibile eseguire un processo il cui unico effetto sia trasferire calore da un corpo più freddo a un corpo più caldo.|1|
Il fisico matematico William Thomson, detto Lord Kelvin, insieme ai contributi del fisico Max Planck, ha affermato l'impossibilità di dispositivi termici con un'efficienza del 100%, poiché ci sarà sempre una perdita di calore.
Non fermarti ora... C'è dell'altro dopo la pubblicità ;)
Applicazioni della seconda legge della termodinamica
La seconda legge della termodinamica si applica ai motori termici e ai frigoriferi.
Seconda legge della termodinamica nelle macchine termico
Al Macchine termiche sono in grado di convertire il calore in lavoro. Una fonte calda fornisce calore al motore termico, che lo trasforma in lavoro. Il resto del calore lo invia alla fonte fredda, come mostrato nell'immagine qui sotto:
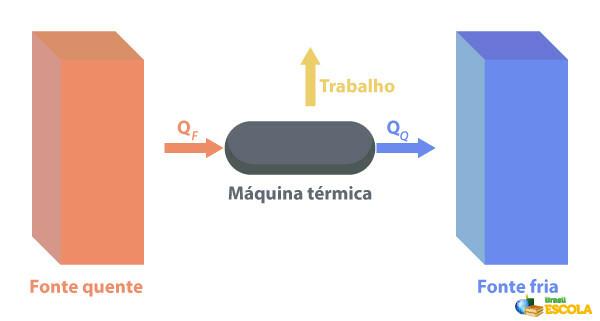
Alcuni esempi di macchine termiche sono: turbine a vapore ea cherosene negli aerei a reazione, motori a combustione, reattori termonucleari.
Seconda legge della termodinamica nei frigoriferi
I frigoriferi sono macchine che Funzionano in modo opposto ai motori termici., dove rimuovono il calore da una regione con temperatura temperatura più bassa e fornirlo a una regione con una temperatura più alta. Poiché ciò non è naturale, è necessario che la macchina esegua un lavoro utilizzando energia elettrica, come descritto nell'immagine seguente:
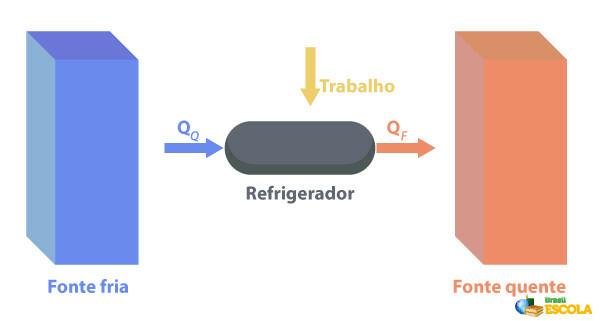
Alcuni esempi di frigoriferi sono frigoriferi e condizionatori d'aria.
Entropia e seconda legge della termodinamica
UN la seconda legge della termodinamica propone l'esistenza dell'entropia, uno quantità fisica responsabile della misurazione del grado di disorganizzazione delle particelle in un sistema fisico o del grado di irreversibilità di processi termodinamici coinvolti nei motori termici, essendo spontaneo, inevitabile, irreversibile e espansivo. Con questo è solo possibile osservare e contenere il grado di volatilità dei processi. All'aumentare dell'entropia, aumenta anche il grado di disordine nel sistema.
UN La nomenclatura dell'entropia è di origine greca e significa "trasformazione"., "cambiamento", essendo così utilizzato in Fisico per indicare casualità e disordine. L'entropia può essere calcolata utilizzando la formula:
\(∆S=\frac{∆U}T\)
\(∆S\) è la variazione di entropia, misurata in [J/K].
\(∆U\) è la variazione di energia interna, misurata in Joule [J].
T è la temperatura, misurata in Kelvin [K].
Da un punto di vista statistico, l'entropia è calcolata dalla formula:
\(S=k\cdot ln\ Ω\)
S è l'entropia, misurata in [J/K].
k è la costante di Boltzmann, vale la pena \(1,4\cdot 10^{-23}\J/K\).
Ω è il numero di possibili microstati per il sistema.
Leggi anche: Processi di propagazione del calore
Formule della seconda legge della termodinamica
Macchine termiche e frigoriferi
\(Q_Q=D+Q_F\)
\(Q_Q\) è il calore della sorgente calda, misurato in Joule [J].
W è il lavoro svolto dal motore termico, misurato in Joule [J].
\(Q_F\) è il calore della sorgente fredda, misurato in Joule [J].
Può essere rappresentato da:
\(W=Q_Q-Q_F\)
W è il lavoro svolto dal motore termico, misurato in Joule [J].
\(Q_Q\) è il calore della sorgente calda, misurato in Joule [J].
\(Q_F\) è il calore della sorgente fredda, misurato in Joule [J].
Frigoriferi
\(η=\frac{Q_F}{Q_Q-Q_F}\)
\(η\) è l'efficienza del frigorifero.
\(Q_F\) è il calore della sorgente fredda, misurato in Joule [J].
\(Q_Q\) è il calore della sorgente calda, misurato in Joule [J].
Può essere rappresentato come:
\(η=\frac{Q_F}W\)
\(η\) è l'efficienza del frigorifero.
\(Q_F\) è il calore della sorgente fredda, misurato in Joule [J].
W è il lavoro svolto dal motore termico, misurato in Joule [J].
Esempi di applicazione delle formule
Esempio 1: Calcolare il lavoro svolto da una macchina termica durante un ciclo che riceve 500 J di calore dalla sorgente calda e cede solo 400 J di calore alla sorgente fredda.
Per calcolare il lavoro di un motore termico, useremo la formula:
\(W=Q_Q-Q_F\)
Sostituendo i valori indicati nel prospetto:
\(L=500-400\)
\(W=100\J\)
Il lavoro del motore termico era di 100 Joule.
Esempio 2: Qual è il rendimento di un frigorifero che riceve 150 J di calore dalla sorgente calda e cede 50 J di calore alla sorgente fredda?
Per calcolare l'efficienza di un frigorifero, useremo la formula:
\(η=\frac{Q_F}{Q_Q-Q_F}\)
Sostituendo i valori indicati nella dichiarazione, otteniamo:
\(η=\frac{50}{150-50}\)
\(η=\frac{50}{100}\)
\(η=0,5\)
Moltiplicando il rendimento per il 100%:
\(η=0.5\cdot100%\)
\(η=50\%\)
Il frigorifero ha un'efficienza del 50%.
Ciclo di Carnot
Il ciclo di Carnot era sviluppato dallo scienziato Sadi Carnot (1796-1832), con l'obiettivo di individuare il massimo rendimento raggiungibile da un motore termico che opera tra una sorgente calda e una sorgente fredda.
Sulla base dei suoi studi, Carnot ha identificato che, per ottenere la massima efficienza da un motore termico, lo è necessario affinché il suo processo fosse reversibile, quindi sviluppò il ciclo di rendimento massimo chiamato ciclo di Carnot, e il Il motore termico che funziona attraverso di esso è chiamato motore termico di Carnot.. Poiché il ciclo di Carnot è reversibile, può essere invertito, ed è così che sono stati sviluppati i frigoriferi.
Il ciclo di Carnot, indipendentemente dalla sostanza utilizzata, è composto da quattro processi descritti nel grafico della pressione per volume (p×V), come possiamo vedere nell'immagine sottostante:
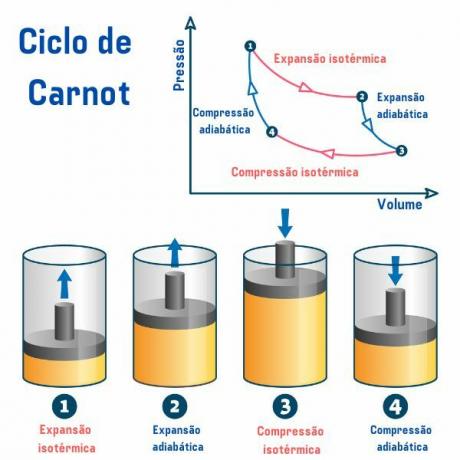
1° processo, dal punto 1 → 2: c'è un'espansione isotermica reversibile (processo in cui la temperatura rimane costante), in cui il gas (o sistema) funziona e acquisisce una quantità di calore dalla sorgente calda.
2° processo, dal punto 2 → 3: c'è un'espansione adiabatica (processo in cui c'è scambio di calore con l'ambiente esterno) reversibile, in cui non c'è scambio di calore calore con fonti termiche, ma il gas funziona e si ha una diminuzione della sua energia interna, provocando una diminuzione della temperatura.
3° processo, dal punto 3 → 4: si verifica una compressione isotermica reversibile, in cui il gas riceve lavoro e cede una quantità di calore alla sorgente fredda.
4° processo, dal punto 4 → 1: si verifica una compressione adibatica reversibile, in cui non avviene alcuno scambio termico con le sorgenti termiche e il gas lo è riscaldato fino a raggiungere la temperatura della fonte calda, e quindi essere posto a contatto con essa, terminando il ciclo.
leggi della termodinamica
Le leggi della termodinamica sono quattro leggi che governano l'intero studio della termodinamica, studiano le relazioni tra volume, temperatura e pressione e altre grandezze fisiche, come il calore e l'energia.
Principio zero della termodinamica: è la legge di equilibrio termico, studia lo scambio di calore tra corpi che hanno temperature diverse.
prima legge della termodinamica: è la legge di conservazione dell'energia nei sistemi termodinamici, studia la trasformazione del calore in lavoro e/o energia interna.
Seconda legge della termodinamica: è la legge che si occupa di motori termici, frigoriferi ed entropia.
Terza legge della termodinamica: è la legge di zero Assoluto, studia gli effetti di questa temperatura.
Leggi anche tu: Prestazioni dei motori termici
Esercizi risolti sulla seconda legge della termodinamica
domanda 1 Determinare la temperatura della sorgente calda di una macchina di Carnot, sapendo che la temperatura della sorgente fredda è 450 K e il suo rendimento è dell'80%.
a) 2250 K
b) 450K
c) 1500K
d) 900K
e) 3640 K
Risoluzione:
Alternativa A. Calcoleremo la temperatura della sorgente calda in base alla formula del rendimento di un motore di Carnot:
\(η=1-\frac{T_F}{T_Q} \)
\(80 \%=1-\frac{450}{T_Q} \)
\(\frac{80}{100}=1-\frac{450}{T_Q} \)
\(0,8=1-\frac{450}{T_Q} \)
\(0,8-1=-\frac{450}{T_Q} \)
\(-0,2=-\frac{450}{T_Q} \)
\(0,2=\frac{450}{T_Q} \)
\(T_Q=\frac{450}{0,2}\)
\(T_Q=2250\ K\)
Domanda 2 (Cefet-PR) Il 2° principio della termodinamica può essere così enunciato: “È impossibile costruire una macchina energia termica che opera in cicli, il cui unico effetto è quello di rimuovere il calore da una fonte e convertirlo integralmente in lavoro". Per estensione, questo principio ci porta a concludere che:
a) È sempre possibile costruire macchine termiche con un rendimento del 100%.
b) qualsiasi motore termico necessita di una sola fonte di calore.
c) calore e lavoro non sono grandezze omogenee.
d) qualsiasi macchina termica trae calore da una fonte calda e respinge parte di quel calore verso una fonte fredda.
e) solo con una sorgente fredda, mantenuta sempre a 0 °C, sarebbe possibile per una certa macchina termica convertire interamente il calore in lavoro.
Risoluzione:
Alternativa D. Questo principio ci informa che è impossibile rimuovere tutto il calore dalla fonte calda e trasferirlo alla fonte fredda.
Nota
|1| Corso di fisica di base: Fluidi, Oscillazioni e Onde, Calore (vol. 2).
Di Pamella Raffaella Melo
Insegnante di Fisica
L'entropia di un sistema non è altro che la misura del suo grado di disorganizzazione. È possibile formulare la Seconda Legge dal concetto di entropia.
Scopri l'affascinante storia dei motori termici e dei loro principali utilizzi.
Sai cosa sono le macchine termiche, i cicli termodinamici e l'efficienza? Ulteriori informazioni su questi importanti concetti di termodinamica.
Accedi al testo e impara la definizione della Prima Legge della Termodinamica, vedi quali sono le formule utilizzate da questa legge e consulta gli esercizi risolti sull'argomento.
Trasformazione isotermica, isovolumetrica e adiabatica. Incontrali!
Sai cos'è la termodinamica? Accedi al testo per scoprire quali sono i concetti più importanti sull'argomento, conoscere le leggi della Termodinamica.