IL teoria dell'ottetto è stato proposto da Newton Lewis, che negli studi ha osservato che avviene l'interazione atomica in modo che ogni elemento acquisisca la stabilità elettronica di un gas nobile, cioè otto elettroni nel strato di valenza. Tuttavia, in alcune molecole, avviene quella che viene chiamata espansione o contrazione dell'ottetto, cioè l'atomo centrale stabilisce legami più o meno previsti.
Leggi anche: Legame covalente - classificazioni e caratteristiche
Come funziona la teoria dell'ottetto?
Naturalmente tutti i sistemi tendono a cercare un modo per acquisire quanta più stabilità possibile, e questo non è diverso con l'atomo. Gli atomi sono "particelle di base" di qualsiasi materia e ognuno ha un'elettrosfera nella sua struttura. Questa elettrosfera è stata divisa da Linus Pauling nei livelli e sottolivelli energetici. Pauling sviluppò un diagramma per dimostrare come sarebbe stata la distribuzione degli elettroni attorno al nucleo di un atomo.
Vedi l'immagine qui sotto:
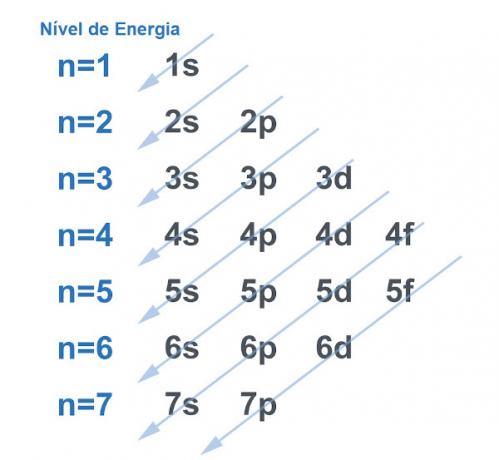
Ogni livello e sottolivello contiene una quantità di elettroni. Facendo un'analogia, possiamo dire che ogni livello è uno scaffale e ogni sottolivello è una scatola. In ogni scatola, inserisci due elettroni. L'atomo è stabile quando tutti i suoi elettroni sono appaiati, cioè quando ci sono tutte le scatole con due elettroni ciascuna.
Esempio:
Facciamo la distribuzione elettronica dell'ossigeno (O), che ha otto elettroni allo stato naturale.
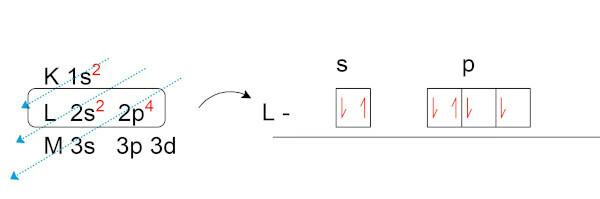
Si noti che, nello strato di valenza (lo strato L, nel sottolivello p), abbiamo due elettroni spaiati. Sono questi elettroni che stabiliscono legami chimici con altri elementi cercando di formare coppie elettroniche.
La teoria dell'ottetto si basa sulla matematica della sommatoria degli elettroni. Se tutti i sottolivelli dell'ultimo guscio elettronico hanno due elettroni ciascuno, il guscio di valenza avrà un totale di otto elettroni e, di conseguenza, l'atomo sarà stabile.
Leggi anche: Numeri quantici - numeri associati alla quantità di energia dell'elettrone
gas nobili
I gas nobili sono gli unici elementi che si trova in natura in forma monoatomica, cioè senza stabilire un legame con un altro atomo. Questo perché sono dotati di stabilità elettronica. Quasi tutti hanno otto elettroni nel guscio di valenza., obbedendo alla regola dell'ottetto, ad eccezione del gas elio, che ha solo due elettroni.

Eccezioni alla teoria dell'ottetto
Alcuni composti riescono a stabilizzarsi con più o meno di otto elettroni nel guscio di valenza. In questi casi, si verificano eccezioni alla teoria dell'ottetto.
espansione dell'ottetto
Succede principalmente con il fosforo (P) e lo zolfo (S), che sono atomi relativamente grandi e hanno il sottolivello "d". In questo caso, l'atomo contiene più di otto elettroni nel suo ultimo guscio.
Esempio:
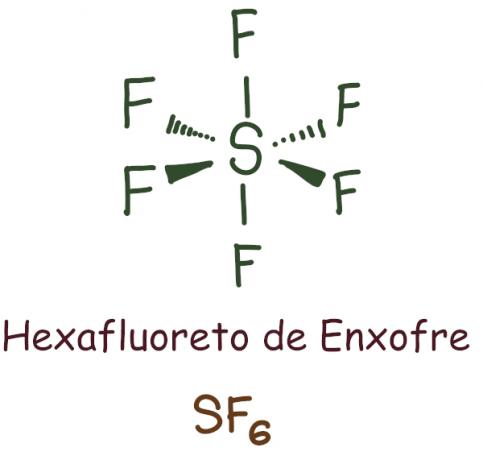
Nel caso dell'esafluoruro di zolfo, l'elemento centrale è stato lasciato con 12 elettroni, superando gli 8 necessari per stabilizzarsi secondo la regola dell'ottetto. In questo caso, c'era un'espansione dell'ottetto.
contrazione dell'ottetto
Succede con berillio (Be), boro (B) e alcuni and ossidi di azoto. Vedi l'esempio:
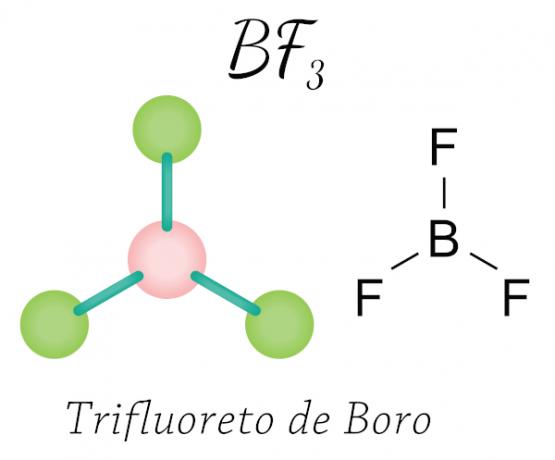
Nel caso del trifluoruro di boro, gli atomi di fluoro acquisiscono gli otto elettroni necessari nel guscio di valenza condividendo elettronico con boro, rispettando la regola dell'ottetto, ma l'atomo centrale (boro) non si stabilizza con sei elettroni, verificandosi così uno contrazione dell'ottetto.
Accedi anche a: Classificazione di un collegamento sigma: quali sono i criteri?
Esercizi risolti
domanda 1 - (Mackenzie-SP) Affinché gli atomi di zolfo e potassio acquisiscano una configurazione elettronica pari a quella di un gas nobile, è necessario che:
(Dati: numero atomico S = 16; K = 19.)
A) lo zolfo riceve 2 elettroni e il potassio riceve 7 elettroni.
B) lo zolfo dà 6 elettroni e il potassio riceve 7 elettroni.
C) lo zolfo produce 2 elettroni e il potassio 1 elettrone.
D) lo zolfo riceve 6 elettroni e il potassio cede 1 elettrone.
E) lo zolfo riceve 2 elettroni e il potassio cede 1 elettrone.
Risoluzione
Alternativa E. Lo zolfo è un elemento della colonna 16 o famiglia 6A. Gli elementi di questa famiglia tendono a ricevere due elettroni per formare coppie elettroniche e hanno un totale di otto elettroni nel guscio di valenza. Gli elementi della famiglia 1A, che sono i metalli alcalini, hanno un solo elettrone nel guscio di valenza. Donando questo elettrone, lo strato precedente diventa lo strato di valenza, già con gli otto elettroni, come dettato dalla regola dell'ottetto.
Domanda 2 - Giudica le seguenti affermazioni come vere (V) o false (F).
I ( ) La regola dell'ottetto afferma che sono necessari otto elettroni nel guscio di valenza affinché l'atomo sia stabile.
II ( ) Lo strato di valenza è il secondo strato elettronico dell'atomo.
III ( ) Il cloro (Cl), della famiglia degli alogeni, tende ad acquisire due elettroni per acquisire stabilità.
IV ( ) Il sodio (Na), elemento della famiglia 1A, tende a perdere l'unico elettrone nel suo guscio di valenza.
Segna l'alternativa corretta:
A) I, III e IV sono veri.
B) I e IV sono veri.
C) Solo II è vero.
D) Solo la IV è falsa.
E) Sono tutte vere.
Risoluzione
Alternativa B. I e IV sono veri. L'affermazione II non è corretta, poiché lo strato di valenza è l'ultimo strato elettronico dell'atomo, non il secondo. E l'affermazione III dice che il cloro tende a guadagnare due elettroni, il che no, poiché il cloro, essendo da 7A o 17, tende ad acquisire un solo elettrone per acquisire così la configurazione elettronica di un gas nobile.
Di Laysa Bernardes Marques de Araújo
Insegnante di chimica
