doppio sale è il nome dato ad una delle classificazioni che il sali inorganici può ricevere. Le altre classificazioni sono: semplice, allume, idrossilato, idrogenato e idratato. Per essere caratterizzato come sale doppio, un sale inorganico deve avere una delle combinazioni descritte di seguito:
Un catione (Y) e due anioni qualsiasi (X e W), ed è rappresentato dalla seguente formula:
YXW
Un anione (X) e due cationi qualsiasi (Y e Z), ed è rappresentato dalla seguente formula:
YZX
Nota: Questi sali si formano quando a reazione di neutralizzazione viene eseguita tra due basi diverso e uno acido, o tra due acidi diversi e una base.
Regola di denominazione per un doppio sale
Per nominare un doppio sale, è necessario, innanzitutto, conoscerne la costituzione, perché, per ogni tipo di sale doppio, esiste una specifica regola di denominazione, come si può vedere di seguito:
a) Regola di nomenclatura per sale doppio con due cationi
Quando uno doppio sale ha due cationi, dobbiamo usare la seguente regola:

Regola di nomenclatura utilizzata per sali doppi con due cationi
Di seguito sono riportati due esempi di applicazione di questa regola di denominazione:
1° Esempio: Linea4S
Questo sale è composto da:
Anione: solfuro (S-2);
Più cationi elettropositivi: litio (Li+1);
Catone meno elettropositivo: ammonio (NH4+1).
Quindi, il suo nome è solfuro di ammonio di litio (doppio).
2° Esempio: RbCaBO3
Questo sale è composto da:
Anione: borato (BO3-3);
Più catione elettropositivo: rubidio (Rb+1);
Catone meno elettropositivo: calcio (Ca+2).
Pertanto, il suo nome è borato (doppio) di rubidio e calcio.
b) Regola di nomenclatura per sale doppio con due anioni
Quando uno doppio sale ha due anioni, dobbiamo usare la seguente regola:
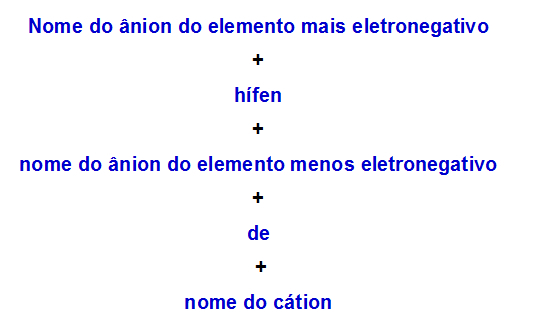
Regola di nomenclatura utilizzata per sali doppi con due anioni
Ecco due esempi di applicazione di questa regola:
1° Esempio: MgFI
Questo sale è composto da:
Cation: magnesio (Mg+2);
Anione più elettronegativo: fluoruro (F-1);
Anione meno elettronegativo: ioduro (I-1).
Pertanto, il suo nome è fluoruro di magnesio-ioduro.
2° Esempio: ZnNO2fratello
Questo sale è composto da:
Cation: zinco (Zn+2);
Anione più elettronegativo: nitrito (NO2-1);
Anione meno elettronegativo: bromuro (Br-1).
Quindi, il suo nome è nitrito di zinco-bromuro.
Assemblaggio della formula di un sale doppio dalla sua nomenclatura
a) Per doppio sale con due cationi
La costruzione della formula di a doppio sale dipende dal conoscerne il nome, che è standardizzato come in tutti i sali, cioè prima il catione e poi l'anione. Poiché il doppio sale può avere due cationi, il loro ordine e la loro collocazione nella formula seguono il nome dato.
1° Esempio: pirofosfato di bario nichel II
Questo sale contiene fosfato (P2oh7), bario (Ba+2) e nichel II (Ni+2), cationi scritti in quella sequenza. Quindi la sua formula è BaNiP2oh7.
2° Esempio: rame II fosfato e oro I
Questo sale ha fosfato (PO4-3), rame II (Cu+2) e oro I (Au+1), cationi scritti in quella sequenza. Pertanto, la sua formula è CuAuPO4.
b) Per sale doppio con due anioni
In caso di doppio sale con due anioni, seguiamo anche, quando poniamo gli anioni nella formula, l'ordine in cui appaiono nel nome dato.
1° Esempio: ioduro di nichel solfato III
Questo sale ha anioni solfato (SO4-2) e ioduro (I-1), scritto in questa sequenza, e il catione nichel III (Ni+3). Quindi la sua formula è NiSO4IO.
2° Esempio: cianuro di piombo fosfato IV
Questo sale ha anioni fosfato (PO4-3) e cianuro (CN-1), scritto in questa sequenza, e il catione piombo IV (Pb+4). Quindi la sua formula è PbPO4CN.
Di Me. Diogo Lopes Dias
Fonte: Scuola Brasile - https://brasilescola.uol.com.br/o-que-e/quimica/o-que-e-um-sal-duplo.htm
